シムツーザ配合錠の添付文書
- 商品名:
- シムツーザ配合錠
- 一般名:
- ダルナビル エタノール付加物・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩配合錠
- 略称 :
- SMT

添付文書の読み方
ここで提供している添付文書情報は、2023年10月現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
抗ウイルス化学療法剤
ダルナビル エタノール付加物・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩配合錠

SYMTUZA® Combination Tablets
- **2025年8月改訂(第3版)
- *2023年8月改訂
- 劇薬
- 処方箋医薬品※
※注意-医師等の処方箋により使用すること
| 日本標準商品分類番号 | 87625 |
|---|
| 貯法 | 室温保存 |
|---|---|
| *有効期間 | 36ヵ月 |
| 承認番号 | 30100AMX00021000 |
|---|---|
| 販売開始 | 2019年7月 |
1. 警告
B型慢性肝炎を合併している患者では、本剤の投与中止により、B型慢性肝炎が再燃するおそれがあるので、本剤の投与を中断する場合には十分注意すること。特に非代償性の場合、重症化するおそれがあるので注意すること。[9.1.3 参照]
2. 禁忌(次の患者には投与しないこと)
2.1
本剤の成分に対し過敏症の既往歴のある患者
**, *2.2
リファンピシン、フェノバルビタール、フェニトイン、ホスフェニトイン、カルバマゼピン、セイヨウオトギリソウ(St. John’s Wort:セント・ジョーンズ・ワート)含有食品、トリアゾラム、ミダゾラム、ピモジド、シンバスタチン、エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン、バルデナフィル、シルデナフィル(レバチオ)、タダラフィル(アドシルカ)、ブロナンセリン、アゼルニジピン、アゼルニジピン・オルメサルタン メドキソミル、ルラシドン、ロミタピド、フィネレノン、ボクロスポリン、イバブラジン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、イサブコナゾニウム硫酸塩、アナモレリン塩酸塩、マバカムテン、リバーロキサバン、チカグレロルを投与中の患者[10.1 参照]
2.3
腎機能あるいは肝機能障害患者で、コルヒチンを投与中の患者[9.2.1、9.3.1、10.2 参照]
2.4
低出生体重児、新生児、乳児、3歳未満の幼児[9.7.1、15.2.2 参照]
3. 組成・性状
3.1 組成
| 販売名 | シムツーザ配合錠 |
|---|---|
| 有効成分 | (1錠中) ダルナビル エタノール付加物867mg(ダルナビルとして800mg)、コビシスタット150mg、エムトリシタビン200mg、テノホビル アラフェナミドフマル酸塩11.2mg(テノホビル アラフェナミドとして10mg) |
| 添加剤 | 二酸化ケイ素、クロスカルメロースナトリウム、ステアリン酸マグネシウム、結晶セルロース、マクロゴール4000、ポリビニルアルコール(部分けん化物)、酸化チタン、タルク、黄色三二酸化鉄 |
3.2 製剤の性状
| 色・剤形 | 黄色~帯黄褐色のフィルムコーティング錠 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 外形 | 表面 | 裏面 | 側面 | |||||||||
 |
 |
 |
||||||||||
| 大きさ | 長径 (mm) |
短径 (mm) |
厚さ (mm) |
重量 (g) |
||||||||
| 22 | 10 | 8 | 1.60 | |||||||||
| 識別コード | JG 8121 | |||||||||||
4. 効能又は効果
HIV-1感染症
5. 効能又は効果に関連する注意
5.1
以下のいずれかのHIV-1感染患者に使用すること。
- 抗HIV薬の治療経験がない患者
- 本剤への切り替え前に、抗HIV薬による治療が6ヵ月間以上変更なく継続され、ウイルス学的抑制(HIV-1 RNA量が50copies/mL未満)が得られており、ダルナビルに対する耐性関連変異を持たず、本剤への切り替えが適切と判断される患者
5.2
本剤による治療にあたっては、患者の治療歴及び可能な場合には薬剤耐性検査(遺伝子型解析あるいは表現型解析)を参考にすること。[17.1.1、17.1.2、18.3.2 参照]
6. 用法及び用量
通常、成人及び12歳以上かつ体重40㎏以上の小児には、1回1錠(ダルナビルとして800mg、コビシスタットとして150mg、エムトリシタビンとして200mg及びテノホビル アラフェナミドとして10mgを含有)を1日1回食事中又は食直後に経口投与する。
7. 用法及び用量に関連する注意
7.1
本剤は、ダルナビル エタノール付加物、コビシスタット、エムトリシタビン及びテノホビル アラフェナミドフマル酸塩の4成分を含有する配合剤であるので、これらの成分を含有する製剤と併用しないこと。また、コビシスタットと同じ薬物動態学的増強因子であるリトナビルを含有する製剤及びテノホビル ジソプロキシルフマル酸塩を含む製剤とも併用しないこと。
7.2
本剤は、HIV-1感染症に対して1剤で治療を行うものであるため、他の抗HIV薬と併用しないこと。また、エムトリシタビンと類似の薬剤耐性、ウイルス学的特性を有しているラミブジンを含む製剤と併用しないこと。
7.3
本剤投与後、クレアチニンクリアランスが30mL/min未満に低下した場合は、投与の中止を考慮すること。[8.3 参照]
8. 重要な基本的注意
*8.1
本剤の使用に際しては、国内外のガイドライン等の最新の情報を参考に、患者又は患者に代わる適切な者に、次の事項についてよく説明し同意を得た後、使用すること。
8.1.1
本剤はHIV感染症の根治療法薬ではないことから、日和見感染を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので、本剤投与開始後の身体状況の変化については、すべて担当医に報告すること。
8.1.2
本剤の長期投与による影響については、現在のところ不明であること。
8.1.3
本剤投与開始後、担当医の指示なしに用量を変更したり、服用を中止したりしないこと。
8.1.4
本剤は併用薬剤と相互作用を起こすことがあるため、服用中のすべての薬剤を担当医に報告すること。また、本剤で治療中に新たに他の薬剤を服用する場合、事前に担当医に相談すること。
8.2
本剤による治療は、抗HIV療法に十分な経験を持つ医師のもとで開始すること。
8.3
本剤投与前は、クレアチニンクリアランス等の腎機能検査を実施し、腎機能障害の有無を確認すること。投与開始時に、クレアチニンクリアランスが30mL/min以上であることを確認すること。また、本剤投与後も定期的な検査等により、患者の状態を注意深く観察すること。[7.3、9.1.4、10.2 参照]
8.4
HIVプロテアーゼ阻害剤による治療中の患者で、糖尿病の発症又は増悪、高血糖が発現し、その中には糖尿病性ケトアシドーシスを合併した例が報告されている。
8.5
ダルナビルの海外臨床試験において、発疹は因果関係の不明なものも含め10.3%の患者に認められ、投与中止を要する発疹は0.5%、発熱及び肝酵素値の上昇を伴う重度の発疹は0.4%、皮膚粘膜眼症候群は0.1%未満に認められた。また、発疹の多くは軽度から中等度であり、投与開始4週以内に発現したが投与継続中に寛解した。なお、治療経験のある患者を対象としたダルナビルの海外臨床試験において、ダルナビル及びラルテグラビルを含むレジメンを使用した場合、ダルナビル又はラルテグラビルの一方を含むレジメンと比較して、薬剤との因果関係が明らかでない皮疹も含めた発疹の発現率が高かった。しかし、薬剤に関連した発疹の発現率には差がなく、発疹は軽度から中等度で治療制限及び投与中止はなかった。
8.6
抗HIV薬の多剤併用療法を行った患者で、免疫再構築症候群が報告されている。投与開始後、免疫機能が回復し、症候性のみならず無症候性日和見感染(マイコバクテリウムアビウムコンプレックス、サイトメガロウイルス、ニューモシスチス等によるもの)等に対する炎症反応が発現することがある。また、免疫機能の回復に伴い自己免疫疾患(甲状腺機能亢進症、多発性筋炎、ギラン・バレー症候群、ブドウ膜炎等)が発現するとの報告があるので、これらの症状を評価し、必要時には適切な治療を考慮すること。
8.7
ダルナビルによる治療中に浮動性めまいが報告されているので、自動車の運転等危険を伴う機械の操作には注意すること。
8.8
エムトリシタビン製剤の臨床試験において皮膚変色が発現し、その発現頻度は有色人種で高いことが示唆されている。
8.9
肝機能障害、黄疸があらわれることがあるので、定期的な肝機能検査を行うなど、観察を十分に行うこと。[11.1.2 参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 血友病患者及び著しい出血傾向を有する患者
HIVプロテアーゼ阻害剤で治療中の血友病患者において、皮膚血腫及び出血性関節症等の出血事象の増加が報告されている。
9.1.2 スルホンアミド系薬剤に過敏症の既往歴のある患者
交叉過敏症があらわれる可能性がある。ダルナビルはスルホンアミド基を有する。
9.1.3 B型肝炎ウイルス(HBV)感染を合併している患者
本剤の投与を中断する場合には十分注意すること。B型慢性肝炎を合併している患者では、本剤の投与中止により、B型慢性肝炎が再燃するおそれがある。特に非代償性の場合、重症化するおそれがある。[1.参照]
9.1.4 腎機能障害のリスクを有する患者
クレアチニンクリアランス及び血清リンの検査を実施すること。[8.3 参照]
9.1.5 病的骨折の既往のある患者又はその他の慢性骨疾患を有する患者
観察を十分に行い、異常が認められた場合には、投与を中止するなど、適切な処置を行うこと。テノホビル アラフェナミドフマル酸塩を含有する製剤の非臨床試験及び臨床試験において、骨密度の低下と骨代謝の生化学マーカーの上昇が認められ、骨代謝の亢進が示唆された。また、抗HIV薬による治療経験がないHIV-1感染症患者に対し、テノホビル アラフェナミドフマル酸塩を含有する製剤が投与された臨床試験において、骨密度が低下した症例が認められた。
9.2 腎機能障害患者
9.2.1 腎機能障害患者で、コルヒチンを投与中の患者
投与しないこと。コルヒチンの血中濃度を上昇させる可能性がある。[2.3、10.2 参照]
9.2.2 重度の腎機能障害のある患者(コルヒチンを投与中の患者を除く)
エムトリシタビンの血中濃度が上昇する[16.6.3 参照]
9.3 肝機能障害患者
9.3.1 肝機能障害患者で、コルヒチンを投与中の患者
投与しないこと。コルヒチンの血中濃度を上昇させる可能性がある。[2.3、10.2 参照]
9.3.2 肝機能障害患者(コルヒチンを投与中の患者を除く)
定期的に肝機能検査を行うなど患者の状態を十分に観察し、悪化が認められた場合には休薬又は投与中止を考慮すること。ダルナビル及びコビシスタットは主に肝臓で代謝され、肝障害患者では高い血中濃度が持続するおそれがある。[16.6.2 参照]
9.3.3 慢性活動性のB型及び/又はC型肝炎患者等投与前に肝機能異常が認められる患者(コルヒチンを投与中の患者を除く)
定期的に肝機能検査を行うなど患者の状態を十分に観察し、悪化が認められた場合には休薬又は投与中止を考慮すること。ダルナビル及びコビシスタットは主に肝臓で代謝され、肝障害患者では高い血中濃度が持続するおそれがある。また、肝機能をさらに悪化させる可能性がある。ダルナビルの海外第IIb/III相試験において、B型及び/又はC型肝炎重複感染患者では、有害事象及び臨床検査値異常のうち、肝酵素の上昇の発現頻度が非重複感染患者より高かった。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、投与しないことが望ましい。本剤投与中に妊娠が判明した場合の代替薬への変更は、変更によるリスクを考慮した上で適切な時期に実施すること。妊娠中期及び妊娠後期の妊婦にダルナビル・コビシスタット配合剤を投与したとき、出産後と比較しダルナビル及びコビシスタットの血中濃度低下が認められている。また、動物試験(サル)においてテノホビルの胎児への移行が報告されている。[16.6.4 参照]
9.6 授乳婦
授乳を避けさせること。ダルナビル1)及びコビシスタット2)は、動物実験(ラット)で乳汁中へ移行することが報告されているが、ヒト乳汁中への移行は不明である。テノホビル及びエムトリシタビンのヒト乳汁中への移行が報告されているが3)、テノホビル アラフェナミドのヒト乳汁中への移行は不明である。また、HIV感染女性患者は、乳児のHIV感染を避けるため、乳児に母乳を与えないことが望ましい。
9.7 小児等
9.7.1
低出生体重児、新生児、乳児、3歳未満の幼児には投与しないこと。[2.4、15.2.2 参照]
9.7.2
3歳~11歳又は体重40kg未満の小児を対象とした臨床試験は実施していない。
9.8 高齢者
患者の肝、腎及び心機能の低下、合併症、併用薬等を十分に考慮すること。
*10. 相互作用
ダルナビル:CYP3Aで代謝され、CYP3A及びCYP2D6を阻害し、またP糖蛋白を阻害する。
コビシスタット:CYP3A及びCYP2D6で代謝され、CYP3A及びCYP2D6を阻害し、またP糖蛋白、BCRP、OATP1B1及びOATP1B3を阻害する。
テノホビル及びエムトリシタビン:糸球体ろ過と能動的な尿細管分泌により腎排泄される。
テノホビル アラフェナミド:カテプシンA、CYP3A及びP糖蛋白の基質である。[16.7.1 参照]
**10.1 併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| リファンピシン リファジン フェノバルビタール フェノバール等 フェニトイン アレビアチン等 ホスフェニトイン ホストイン カルバマゼピン テグレトール [2.2、16.7.2 参照] |
ダルナビル、コビシスタット及びテノホビル アラフェナミドの血中濃度が低下し、本剤の効果が減弱するおそれがある。 | これらの薬剤のCYP3A及びP糖蛋白誘導作用による。 |
| セイヨウオトギリソウ(St. John’s Wort、セント・ジョーンズ・ワート)含有食品 [2.2 参照] |
||
| トリアゾラム ハルシオン ミダゾラム ドルミカム ミダフレッサ ブコラム [2.2、16.7.2 参照] |
これらの薬剤の血中濃度上昇により、過度の鎮静や呼吸抑制等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | ダルナビル及びコビシスタットのCYP3A阻害作用により、これらの薬剤の代謝が阻害される。 |
| ピモジド [2.2 参照] |
ピモジドの血中濃度上昇により、不整脈等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | |
| シンバスタチン リポバス [2.2 参照] |
シンバスタチンの血中濃度上昇により、横紋筋融解症が起こる可能性がある。 | |
| エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン クリアミン ジヒドロエルゴタミン ジヒデルゴット エルゴメトリン メチルエルゴメトリン パルタンM [2.2 参照] |
これらの薬剤の血中濃度上昇により、末梢血管痙縮、虚血等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | |
| バルデナフィル レビトラ シルデナフィル レバチオ タダラフィル アドシルカ [2.2 参照] |
これらの薬剤の血中濃度を上昇させるおそれがある。 | |
| ブロナンセリン ロナセン [2.2 参照] |
ブロナンセリンの血中濃度が上昇し、作用が増強するおそれがある。 | |
| アゼルニジピン カルブロック アゼルニジピン・オルメサルタン メドキソミル レザルタス配合錠 [2.2 参照] |
アゼルニジピンの血中濃度が上昇し、作用が増強するおそれがある。 | |
| ルラシドン ラツーダ [2.2 参照] |
ルラシドンの血中濃度が上昇し、作用が増強するおそれがある。 | |
| ロミタピド ジャクスタピッド [2.2 参照] |
ロミタピドの血中濃度が著しく上昇するおそれがある。 | |
| *フィネレノン ケレンディア [2.2 参照] |
フィネレノンの血中濃度が著しく上昇するおそれがある。 | |
| **ボクロスポリン ルプキネス [2.2 参照] |
ボクロスポリンの血中濃度が上昇し、作用が増強するおそれがある。 | |
| イバブラジン コララン [2.2 参照] |
イバブラジンの血中濃度が上昇し、過度の徐脈があらわれることがある。 | コビシスタットのCYP3A阻害作用により、これらの薬剤の代謝が阻害される。 |
| ベネトクラクス (再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期) ベネクレクスタ [2.2 参照] |
ベネトクラクスの血中濃度が上昇し、腫瘍崩壊症候群の発現が増強する可能性がある。 | |
| *イサブコナゾニウム硫酸塩 クレセンバ [2.2 参照] |
イサブコナゾールの血中濃度が上昇し、作用が増強するおそれがある。 | |
| **アナモレリン塩酸塩 エドルミズ [2.2 参照] |
アナモレリンの血中濃度が上昇し、副作用の発現が増強するおそれがある。 | |
| **マバカムテン カムザイオス [2.2 参照] |
マバカムテンの血中濃度が上昇し、副作用が増強され、収縮機能障害による心不全のリスクが高まるおそれがある。 | |
| リバーロキサバン イグザレルト チカグレロル ブリリンタ [2.2 参照] |
これらの薬剤の血中濃度が上昇し、作用が増強されることにより、出血の危険性が増大するおそれがある。 | ダルナビル及びコビシスタットのCYP3A阻害作用又はP糖蛋白阻害作用により、これらの薬剤の血中濃度が上昇することがある。 |
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| デキサメタゾン(全身投与) | ダルナビル及びコビシスタットの血中濃度が低下し、本剤の効果が減弱するおそれがある。併用する場合には注意して投与すること。 | デキサメタゾンのCYP3A誘導作用により、ダルナビル及びコビシスタットの代謝が促進される。 |
| アトルバスタチン [16.7.2 参照] |
アトルバスタチンの血中濃度上昇により、横紋筋融解症が起こる可能性がある。併用する場合には必要に応じてアトルバスタチンの投与量を減量するなど注意して投与すること。 | ダルナビル及びコビシスタットのCYP3A阻害作用により、これらの薬剤の代謝が阻害される。 |
| サルメテロール | サルメテロールの血中濃度上昇により、QT延長、動悸、洞性頻脈等の心血管系事象の発現リスクが増大する可能性がある。併用する場合には必要に応じてサルメテロールの投与量を減量するなど注意して投与すること。 | |
| シルデナフィル バイアグラ タダラフィル シアリス、ザルティア [16.7.2 参照] |
これらの薬剤の血中濃度を上昇させる可能性がある。併用する場合には必要に応じてこれらの薬剤の投与量を減量するなど注意して投与すること。 | |
| クロラゼプ酸 ジアゼパム エスタゾラム フルラゼパム ゾルピデム |
||
| アミオダロン ベプリジル ジソピラミド リドカイン(全身投与) キニジン |
||
| シクロスポリン タクロリムス シロリムス テムシロリムス [16.7.2 参照] |
||
| クロナゼパム エトスクシミド |
||
| Ca拮抗剤 (フェロジピン、 ニフェジピン、 ニカルジピン、 アムロジピン、 ジルチアゼム、 ベラパミル等) |
||
| フルチカゾン ブデソニド プレドニゾロン |
||
| ダサチニブ エベロリムス ニロチニブ ラパチニブ ビンブラスチン ビンクリスチン |
||
| ボセンタン | ||
| アピキサバン | ||
| エプレレノン | ||
| トルバプタン エレトリプタン |
||
| *ダビガトランエテキシラート [16.7.2 参照] |
ダルナビル及びコビシスタットのP糖蛋白阻害作用による。 | |
| アミトリプチリン イミプラミン パロキセチン ノルトリプチリン セルトラリン トラゾドン [16.7.2 参照] |
ダルナビル及びコビシスタットのCYP3A又はCYP2D6阻害作用により、これらの薬剤の代謝が阻害される。 | |
| リスペリドン ペルフェナジン クエチアピン |
||
| フェンタニル オキシコドン トラマドール |
||
| プロパフェノン | ||
| トルテロジン | ||
| デキストロメトルファン [16.7.2 参照] |
||
| ベネトクラクス (再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の維持投与期、急性骨髄性白血病) |
ベネトクラクスの血中濃度が上昇し、副作用が増強するおそれがあるので、ベネトクラクスを減量するとともに患者の状態を慎重に観察すること。 | コビシスタットのCYP3A阻害作用により、これらの薬剤の代謝が阻害される。 |
| カルベジロール メトプロロール チモロール |
これらの薬剤の血中濃度を上昇させる可能性がある。併用する場合には必要に応じてこれらの薬剤の投与量を減量するなど注意して投与すること。 | コビシスタットのCYP2D6阻害作用により、これらの薬剤の代謝が阻害される。 |
| フレカイニド メキシレチン |
コビシスタットのCYP2D6阻害作用により、これらの薬剤の代謝が阻害される。 | |
| ロスバスタチン プラバスタチン ピタバスタチン [16.7.2 参照] |
これらの薬剤の血中濃度上昇により、横紋筋融解症が起こる可能性がある。併用する場合には必要に応じてこれらの薬剤の投与量を減量するなど注意して投与すること。 | 機序不明 |
| ジゴキシン [16.7.2 参照] |
ジゴキシンの血中濃度を上昇させる可能性がある。併用する場合には必要に応じてジゴキシンの投与量を減量するなど注意して投与すること。 | ダルナビル及びコビシスタットのP糖蛋白阻害作用による。 |
| コルヒチン [2.3、9.2.1、9.3.1 参照] |
コルヒチンの血中濃度を上昇させる可能性がある。併用する場合には必要に応じてコルヒチンの投与量を減量するなど注意して投与すること。 | ダルナビル及びコビシスタットのCYP3A阻害作用又はP糖蛋白阻害作用による。 |
| グレカプレビル・ピブレンタスビル | グレカプレビルの血中濃度を上昇させる可能性がある。併用する場合には必要に応じてグレカプレビル・ピブレンタスビルの投与量を減量するなど注意して投与すること。 | ダルナビル及びコビシスタットのP糖蛋白、BCRP又はOATP1B阻害作用による。 |
| ドロスピレノン | ドロスピレノンの血中濃度を上昇させる可能性がある。併用する場合には必要に応じてドロスピレノンの投与量を減量するなど注意して投与すること。 | 機序不明 |
| 経口避妊剤 (エチニルエストラジオール、ノルエチステロン等) [16.7.2 参照] |
これらの薬剤の血中濃度を低下させる可能性がある。本剤を投与する場合は、別の避妊方法を行うことが望ましい。 | 機序不明 |
| メサドン [16.7.2 参照] |
メサドンの血中濃度を低下させる可能性がある。併用する場合には注意して投与すること。 | 機序不明 |
| リファブチン [16.7.2 参照] |
ダルナビル、コビシスタット及びテノホビル アラフェナミドの血中濃度が低下し、本剤の効果が減弱するおそれがある。また、リファブチンの血中濃度を上昇させる可能性がある。併用する場合には必要に応じて本剤又はリファブチンの投与量を調節するなど注意して投与すること。 | リファブチンのCYP3A及びP糖蛋白誘導作用、及びダルナビル及びコビシスタットのCYP3A阻害作用による。 |
| クラリスロマイシン エリスロマイシン [16.7.2 参照] |
ダルナビル、コビシスタット又はこれらの薬剤の血中濃度が上昇する可能性がある。併用する場合には必要に応じて本剤又はこれらの薬剤の投与量を調節するなど注意して投与すること。 | ダルナビル及びコビシスタットとこれらの薬剤のCYP3A阻害作用により、相互に代謝が阻害される。 |
| イトラコナゾール ケトコナゾール注) ボリコナゾール フルコナゾール [16.7.2 参照] |
ダルナビル、コビシスタット、テノホビル アラフェナミド又はこれらの薬剤の血中濃度が上昇する可能性がある。併用する場合には必要に応じて本剤又はこれらの薬剤の投与量を調節するなど注意して投与すること。 | ダルナビル、コビシスタット及びテノホビル アラフェナミドとこれらの薬剤のCYP3A及びP糖蛋白阻害作用による。 |
| ワルファリン [16.7.2 参照] |
ワルファリンの血中濃度に影響を与えることがある。併用する場合には必要に応じて本剤又はワルファリンの投与量を調節するなど注意して投与すること。 | ダルナビル及びコビシスタットの薬物代謝酵素阻害作用により、血中濃度に変化がおこることがある。 |
| アシクロビル バラシクロビル ガンシクロビル バルガンシクロビル等 |
これらの薬剤、テノホビル又はエムトリシタビンの血中濃度が上昇し、有害事象を増強する可能性がある。併用する場合には必要に応じて本剤又はこれらの薬剤の投与量を調節するなど注意して投与すること。 | 尿細管への能動輸送により排泄される薬剤と併用する場合、排泄経路の競合により排泄が遅延する。 |
| 腎毒性を有する薬剤 [8.3、11.1.4 参照] |
これらの薬剤との併用は避けることが望ましい。 | これらの薬剤との併用により血中濃度が上昇するおそれがある。 |
注)国内では外用剤のみ発売
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、多形紅斑(頻度不明)、急性汎発性発疹性膿疱症(頻度不明)
重度の発疹があらわれた場合は、本剤の投与を直ちに中止し適切な処置を行うこと。
11.1.2 肝機能障害(頻度不明)、黄疸(頻度不明)
AST、ALT、γ-GTPの上昇等を伴う肝機能障害、黄疸があらわれることがある。[8.9 参照]
11.1.3 急性膵炎(0.1%)
11.1.4 腎不全又は重度の腎機能障害(頻度不明)
腎機能不全、腎不全、急性腎障害、近位腎尿細管機能障害、ファンコニー症候群、急性腎尿細管壊死、腎性尿崩症又は腎炎等の重度の腎機能障害があらわれることがある。臨床検査値に異常が認められた場合には、投与を中止するなど、適切な処置を行うこと。特に腎機能障害の既往がある患者や腎毒性のある薬剤が投与されている患者では注意すること。[10.2 参照]
11.1.5 乳酸アシドーシス及び脂肪沈着による重度の肝腫大(脂肪肝)(頻度不明)
乳酸アシドーシス又は肝細胞毒性が疑われる臨床症状又は検査値異常(アミノトランスフェラーゼの急激な上昇等)が認められた場合には、本剤の投与を一時中止すること。特に肝疾患の危険因子を有する患者においては注意すること。エムトリシタビン又はテノホビルを含む核酸系逆転写酵素阻害薬の単独投与又はこれらの併用療法により、重篤な乳酸アシドーシス及び脂肪沈着による重度の肝腫大(脂肪肝)が、女性に多く報告されている。
11.2 その他の副作用
| 5%以上 | 5%未満 | 頻度不明 | |
|---|---|---|---|
| 免疫系障害 | 過敏症、免疫再構築症候群 | ||
| 代謝及び栄養障害 | 糖尿病、食欲不振、体脂肪の再分布/蓄積 | 高トリグリセリド血症、高コレステロール血症、高脂血症 | |
| 精神障害 | 異常な夢 | ||
| 神経系障害 | 頭痛 | ||
| 胃腸障害 | 下痢、腹痛 | 悪心、嘔吐、消化不良、腹部膨満、鼓腸 | 膵酵素増加 |
| 肝胆道系障害 | 急性肝炎、肝酵素増加 | ||
| 皮膚及び皮下組織障害 | 発疹 | そう痒症、蕁麻疹、血管性浮腫 | |
| 筋骨格系及び結合組織障害 | 筋肉痛、骨壊死 | ||
| 生殖系及び乳房障害 | 女性化乳房 | ||
| 全身障害及び投与局所様態 | 疲労、無力症 | ||
| 臨床検査 | 総コレステロール増加、LDLコレステロール増加、トリグリセリド増加、ブドウ糖増加、AST増加、ALT増加、膵型アミラーゼ増加、血中クレアチニン増加 | ALP増加 | リパーゼ増加 |
13. 過量投与
13.1 処置
ダルナビル及びコビシスタットは血漿蛋白結合率が高いため、透析により除去されないと考えられる。エムトリシタビン及びテノホビルは血液透析により一部除去される。
14. 適用上の注意
14.1 薬剤調製時の注意
本剤を粉砕して使用しないこと。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1
健康被験者あるいは軽度から中等度の腎機能障害を有する被験者の腎機能(GFR)に及ぼすコビシスタットの影響を検討した。イオヘキソールクリアランスは変化がなかったが、血清クレアチニン値を用いた推算クレアチニンクリアランス及び24時間内因性クレアチニンクリアランスはプラセボに比べ最大で約28%低下した。なお、健康被験者で腎血漿流量を測定したところ、変化はなかった。
15.2 非臨床試験に基づく情報
15.2.1
ダルナビルの動物実験(ラット)4)~6)では、造血系、血液凝固系、肝、腎、膵臓及び甲状腺に影響が認められた。活性化部分トロンボプラスチン時間の延長とともに、赤血球パラメータのわずかな減少がみられた。
15.2.2
生後23から26日(ヒトの3歳未満に相当)まで、幼若ラットにダルナビルを20mg/kgから1000mg/kgの用量で投与した結果、死亡例が認められた。[2.4、9.7.1 参照]
15.2.3
マウス7)及びラット8)を用いたダルナビルのがん原性試験の結果、雌雄に用量依存的な肝細胞腺腫及び肝細胞癌の発現率の増加、雄ラットに甲状腺濾胞細胞腺腫が認められた。
16. 薬物動態
16.1 血中濃度
*16.1.1 単回投与
健康成人8例に本剤を食後に単回経口投与したときの血漿中ダルナビル及びコビシスタット、エムトリシタビン、テノホビル アラフェナミドの薬物動態パラメータを表1に示す9)。
| 薬物動態 パラメータ |
平均値(標準偏差)、tmax:中央値(範囲) | |||
|---|---|---|---|---|
| 8例 | 8例 | 8例 | 8例 | |
| ダルナビル | コビシスタット | エムトリシタビン | テノホビル アラフェナミド | |
| tmax (hr) |
3.00 (1.50-4.00) |
2.50 (2.00-4.00) |
1.75 (1.00-3.00) |
1.25 (0.75-2.50) |
| Cmax (ng/mL) |
5965 (958) |
1094 (273) |
2671 (431) |
183 (71.2) |
| AUC∞ (ng・hr/mL) |
58441 (20276) |
7325 (2754) |
11342 (1262) |
132 (38.4) |
| t1/2 (hr) |
6.39 (2.41) |
3.69 (0.70) |
18.71 (2.97) |
0.26 (0.06) |
健康成人96例に本剤を食後に単回投与したときの血漿中ダルナビル及びコビシスタット、エムトリシタビン、テノホビル アラフェナミドの薬物動態パラメータを表2に示す10)。(外国人データ)
| 薬物動態 パラメータ |
平均値(標準偏差)、tmax:中央値(範囲) | |||
|---|---|---|---|---|
| 93例 | 93例 | 93例 | 94例 | |
| ダルナビル | コビシスタット | エムトリシタビン | テノホビル アラフェナミド | |
| tmax (hr) |
4.00 (1.50-8.00) |
4.00 (1.50-6.00) |
2.00 (0.60-5.00) |
1.50 (0.25-3.50) |
| Cmax (ng/mL) |
7042 (1481) |
894 (254) |
2041 (481) |
110 (54.1) |
| AUC∞ (ng・hr/mL) |
87280注1) (28097) |
6785 (2518) |
11882注2) (2002) |
127注3) (39.4) |
| t1/2 (hr) |
5.9注1) (2.1) |
3.7 (0.7) |
16.5注2) (3.3) |
0.3注3) (0.1) |
注1)87例
注2)85例
注3)79例
16.1.2 反復投与
健康成人10例に本剤を1日1回食後に反復経口投与したときの血漿中ダルナビル及びコビシスタット、エムトリシタビン、テノホビル アラフェナミドの薬物動態パラメータ(12日目)を表3に示す11)。(外国人データ)
| 薬物動態 パラメータ |
平均値(標準偏差)、tmax, t1/2:中央値(範囲) | |||
|---|---|---|---|---|
| 10例 | ||||
| ダルナビル | コビシスタット | エムトリシタビン | テノホビル アラフェナミド | |
| tmax (hr) |
3.00 (3.00-4.00) |
3.00 (2.00-4.00) |
1.75 (1.50-2.00) |
0.50 (0.50-1.00) |
| Cmax (ng/mL) |
9743.2 (1391.01) |
1305.2 (179.95) |
2198.9 (455.01) |
130.7 (51.19) |
| AUCtau (ng・hr/mL) |
113654.8 (27016.15) |
10097.3 (2395.47) |
12602.1 (2067.52) |
- |
| AUClast (ng・hr/mL) |
- | - | - | 116.4 (30.27) |
| t1/2 (hr) |
7.13 (6.53-9.01) |
2.90 (2.81-3.42) |
5.48 (4.74-6.96) |
0.41 (0.33-0.51) |
抗HIV薬の治療経験がない成人HIV感染症患者又はダルナビル、エムトリシタビン、テノホビル アラフェナミド耐性関連変異を持たない抗HIV薬既治療のHIV感染患者21例に、本剤を1日1回食後に反復投与したときの血漿中ダルナビル及びコビシスタット、エムトリシタビン、テノホビル アラフェナミドの定常状態における薬物動態パラメータを表4に示す12)。(外国人データ)
| 薬物動態 パラメータ |
平均値(変動係数)、tmax, t1/2:中央値(範囲) | |||
|---|---|---|---|---|
| 21例 | ||||
| ダルナビル | コビシスタット | エムトリシタビン | テノホビル アラフェナミド | |
| tmax (hr) |
3.00 (2.00-4.00) |
3.03 (3.00-4.00) |
1.52 (1.50-2.00) |
0.53 (0.50-1.00) |
| Cmax (ng/mL) |
8826.2 (33.3) |
1128.7 (35.3) |
2056.4 (25.3) |
163.0 (51.9) |
| AUCtau (ng・hr/mL) |
99301.8 (45.3) |
8744.5 (43.9) |
11918.0 (35.9) |
- |
| AUClast (ng・hr/mL) |
- | - | - | 130.5 (34.1) |
| t1/2 (hr) |
9.42 (6.31-13.87) |
3.16 (2.77-3.70) |
7.51 (6.40-8.79) |
0.45 (0.38-0.66) |
16.2 吸収
16.2.1 食事の影響
本剤を空腹時に投与した結果、ダルナビルのAUClast及びCmaxは高脂肪食と共に投与した時と比較してそれぞれ34%及び45%低く、コビシスタットのAUClast及びCmaxは高脂肪食と共に投与した時と比較してそれぞれ29%及び23%低かった。また、エムトリシタビンのCmaxは高脂肪食と共に投与した時と比較して、空腹時に投与した時の方が26%高く、AUClastは同程度であった。テノホビル アラフェナミドのCmaxは高脂肪食と共に投与した時と比較して、空腹時に投与した時の方が82%高く、AUClastは同程度であった。なお、食事の内容は、AUC及びCmaxの変動の程度には影響しない。13)(外国人データ)
16.3 分布
16.3.1 ダルナビル
ヒト血漿蛋白結合率は約95%であり、主にα1-酸性糖蛋白に結合した14)。(in vitro試験、平衡透析法)
16.3.2 コビシスタット
ヒト血漿蛋白結合率は、97~98%であった15)、16)。(ex vivo試験、平衡透析法)
16.3.3 エムトリシタビン
ヒト血漿蛋白結合率は、0.02〜200μg/mLの濃度範囲において濃度に依存せず4%未満であった。
16.3.4 テノホビル アラフェナミド
ヒト血漿蛋白結合率は、77〜86%であった。
16.4 代謝
16.4.1 ダルナビル
ヒト肝ミクロソームを用いたin vitro試験で、ダルナビルは主にCYP3A4により酸化的に代謝されることが示唆された。In vivo試験よりダルナビルの主な代謝物は3種類あり、野生型HIV株に対する活性はいずれも未変化体の10%以下であった。健康成人に14C標識したダルナビル/リトナビル400/100mgを単回経口投与したとき、血漿中放射能の大部分は未変化体由来であることが示された。17)
16.4.2 コビシスタット
ヒト肝ミクロソーム及びCYPアイソザイムを用いたin vitro試験で、コビシスタットは主にCYP3Aにより酸化的に代謝され、一部CYP2D6で代謝されることが示唆された。また、グルクロン酸抱合体は検出されなかった。18)、19)
16.4.3 エムトリシタビン
エムトリシタビンは主に尿中に排泄され、代謝の影響をほとんど受けない。
16.4.4 テノホビル アラフェナミド
経口投与後、末梢血単核球及びマクロファージのカテプシンA及び肝細胞のカルボキシルエステラーゼ1によりテノホビルに代謝され、その後、テノホビル二リン酸に代謝された。CYP分子種発現系酵素を用いた検討において、テノホビル アラフェナミドはCYP3Aでわずかに代謝された。
16.5 排泄
16.5.1 ダルナビル
健康成人に14C標識したダルナビル/リトナビル400/100mgを単回経口投与したとき、投与放射能の約79.5%が糞中に、約13.9%が尿中に排泄された。また、未変化体の排泄率は、糞中が約41.2%、尿中が約7.7%であった。ダルナビル150mgを単独で静脈内投与したときの全身クリアランスは32.8L/h(平均値)であり、リトナビル100mgと併用したときの全身クリアランスは5.9L/h(平均値)であった。本剤を投与したときのダルナビルの消失半減期は、約6~7時間(中央値)であった。10)、11)、20)、21)(外国人データ)
16.5.2 コビシスタット
コビシスタット150mgを6日間反復投与した後に14C-コビシスタット150mgを経口投与したところ、投与量の86.2%(平均値)が糞中に、8.2%(平均値)が尿中に排泄された。経口投与後のコビシスタットの消失半減期は、約3~4時間(中央値)であった。22)(外国人データ)
16.5.3 エムトリシタビン
健康被験者にエムトリシタビン200mgを反復投与後14C-エムトリシタビンを単回投与したところ、投与量の86%は尿中に、14%は糞中に回収された。また、14C-エムトリシタビンを単回投与したところ、投与量の13%の代謝物がヒト尿中に検出された。腎クリアランスが推定クレアチニンクリアランスを上回ったことから、糸球体ろ過と尿細管への能動輸送の両方による排泄が示唆された。(外国人データ)
16.5.4 テノホビル アラフェナミド
健康被験者に14C-テノホビル アラフェナミドフマル酸塩25mgを単回投与したところ、投与量の47.2%が糞中に、36.2%が尿中に排泄された。その主成分はテノホビルであり、糞中の99%、尿中の86%を占めた。また、投与量の1.4%がテノホビル アラフェナミドとして尿中に排泄された。テノホビルは腎臓での糸球体ろ過と尿細管への能動輸送の両方により排泄された。(外国人データ)
16.6 特定の背景を有する患者
16.6.1 小児HIV-1感染患者
本剤を用いた小児HIV-1感染患者を対象とした試験は実施していない。
(1)ダルナビル
12歳以上18歳未満で体重40kg以上の小児HIV-1感染患者を対象とし、2剤のNRTIを併用したダルナビル及びリトナビル(800/100mg)の非盲検試験における、小児HIV-1感染患者のダルナビルの薬物動態パラメータを表5に示す23)。(外国人データ)
| 薬物動態 |
平均値(標準偏差)、 |
|---|---|
| 12例 | |
| tmax (hr) |
3.00 (1.00-6.00) |
| Cmax (ng/mL) |
6721 (1700) |
| Cmin (ng/mL) |
1589 (768.2)注1) |
| AUC24h (ng・hr/mL) |
81880 (26300)注1) |
注1)10例
(2)コビシスタット、エムトリシタビン及びテノホビル アラフェナミド
12歳以上18歳未満で体重35kg以上の小児HIV-1感染患者を対象としたエルビテグラビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミドフマル酸塩配合剤(150・150・200・10mg)の非盲検試験における、小児HIV-1感染患者のコビシスタット、エムトリシタビン、テノホビル アラフェナミド及びテノホビルの薬物動態パラメータを表6に示す。(外国人データ)
| 薬物動態 |
平均値(変動係数)、 |
|||
|---|---|---|---|---|
| 24例 | ||||
| コビシスタット | エムトリシタビン | テノホビル アラフェナミド | テノホビル | |
| tmax (hr) |
4.00 (2.01-5.00) |
2.00 (1.00-4.00) |
1.48 (0.50-2.00) |
3.00 (1.00-4.00) |
| Cmax (ng/mL) |
1202 (35.0) |
2265 (22.5) |
167 (64.4) |
18 (23.7) |
| AUCtau (ng・hr/mL) |
8241 (36.1)注1) |
14424 (23.9) |
- | 288 (18.8)注1) |
| AUClast (ng・hr/mL) |
- | - | 189 (55.8) |
- |
注1)23例
16.6.2 肝機能障害患者
(1)ダルナビル
軽度(Child-Pugh分類クラスA、8例)及び中等度肝障害患者(Child-Pugh分類クラスB、8例)にダルナビル/リトナビル600/100mgを1日2回反復投与したときのダルナビルの薬物動態を健康被験者と比較したとき、顕著な差は認められなかった24)。なお、重度肝障害患者(Child-Pugh分類クラスC)を対象とした試験は実施していない。(外国人データ)[9.3.2 参照]
(2)コビシスタット
中等度の肝機能障害(Child-Pugh分類クラスB)を有する被験者において、コビシスタット150mg投与時の薬物動態を健康被験者と比較したとき、顕著な差は認められなかった。なお、重度肝障害患者(Child-Pugh分類クラスC)を対象とした試験は実施していない。(外国人データ)[9.3.2 参照]
(3)エムトリシタビン
肝機能障害患者を対象とした試験は実施していない。
(4)テノホビル アラフェナミド
軽度肝障害患者(Child-Pugh分類クラスA)及び中等度肝障害患者(Child-Pugh分類クラスB)にテノホビル アラフェナミド25mgを単回投与したときのテノホビル アラフェナミド及びテノホビルの薬物動態を健康被験者と比較したとき、顕著な差は認められなかった。なお、重度肝障害患者(Child-Pugh分類クラスC)を対象とした試験は実施していない。(外国人データ)
16.6.3 腎機能障害患者
(1)ダルナビル
中等度腎障害(CLCRが30~60mL/min)を有するHIV-1感染患者(20例)において、腎機能の低下によりダルナビル600mgの薬物動態に有意な影響がないことが示された。重度腎障害又は末期腎疾患を有するHIV-1感染患者における試験は実施されていない。(外国人データ)
(2)コビシスタット
重度腎障害(CLCRが30mL/min未満)を有する被験者において、コビシスタット150mgの薬物動態を検討した。コビシスタットの薬物動態を健康被験者と比較したとき、顕著な差は認められなかった。(外国人データ)
(3)エムトリシタビン
重度腎機能障害を有する被験者(CLCRが30mL/min未満)における、エムトリシタビン200mg単回投与時のエムトリシタビンのCmax及びAUCは、CLCRが80mL/min超の被験者に対し、それぞれ約30%及び約200%上昇した。(外国人データ)[9.2.2 参照]
(4)テノホビル アラフェナミド
重度腎機能障害を有する被験者(CLCRが15mL/min以上30mL/min未満の非透析患者)における、テノホビル アラフェナミド25mg単回投与時のテノホビル アラフェナミドのCmax及びAUCは、CLCRが90mL/min超の被験者に対してそれぞれ79%及び92%上昇し、テノホビルのCmax及びAUCは、それぞれ179%及び474%上昇した。CLCRが15mL/min未満の腎機能障害を有する被験者における薬物動態は検討していない。(外国人データ)
16.6.4 妊婦、産婦
妊娠中期のHIV感染患者(7例)に、ダルナビル・コビシスタット配合剤(800・150mg)を1日1回投与したとき、ダルナビルのCmax、AUC24h及びCminは、出産後(6~12週;6例)と比較してそれぞれ49%、56%及び92%減少した。妊娠後期(6例)では、ダルナビルのCmax、AUC24h及びCminはそれぞれ37%、50%及び89%減少した25)。(外国人データ)[9.5 参照]
16.7 薬物相互作用
16.7.1 In vitro試験成績
(1)ダルナビル
CYP3Aで代謝され、CYP3A(Ki:0.4μmol/L)及びCYP2D6(Ki:41μmol/L)を阻害し、またP糖蛋白(IC50:32.9μmol/L)を阻害する26)、27)。[10.参照]
(2)コビシスタット
CYP3A及びCYP2D6で代謝され、CYP3A(IC50:0.03~0.29μmol/L)及びCYP2D6(IC50:9.17μmol/L)を阻害し、またP糖蛋白、BCRP(IC50:59μmol/L)、OATP1B1(IC50:3.50μmol/L)、OATP1B3(IC50:1.88μmol/L)及びMATE1(IC50:1.87μmol/L)を阻害する28)~32)。[10.参照]
(3)エムトリシタビン
OAT3の基質である。
(4)テノホビル アラフェナミド
CYP3Aで代謝される。P糖蛋白、BCRP、OATP1B1及びOATP1B3の基質である。[10.参照]
(5)テノホビル
OAT1、OAT3及びMRP4の基質であり、OAT1に対する阻害作用(IC50:29.3μmol/L)は弱かった。
*16.7.2 臨床成績
本剤を用いた薬物相互作用試験は実施されていないため、ダルナビル・コビシスタット配合剤、ダルナビル、コビシスタット、エムトリシタビン、テノホビル アラフェナミドを用いた試験成績を示す。
**(1)ダルナビル・コビシスタット配合剤
ダルナビル・コビシスタット配合剤が併用薬の薬物動態に及ぼす影響について表7に示す。[10.2 参照]
| 併用薬 | 併用薬の 用法・用量 |
ダルナビル・コビシスタット配合剤の 用法・用量 |
例数 | 併用薬の薬物動態パラメータ: [90%信頼区間] |
|
|---|---|---|---|---|---|
| Cmax | AUC∞ | ||||
| ダビガトランエテキシラート | 150mg 単回 |
ダルナビル・コビシスタット 800・150mg 単回 |
14 | 2.64 [2.29, 3.05] |
2.64 [2.32, 3.00] |
| ダルナビル・コビシスタット 800・150mg 1日1回注1) |
14 | 1.99 [1.72, 2.30] |
1.88 [1.65, 2.13] |
||
注1)ダルナビル・コビシスタット800・150mgを1日1回17日間反復経口投与し、投与15日目にダビガトランエテキシラート150mgを単回経口投与
**(2)ダルナビル
併用薬がダルナビルの薬物動態に及ぼす影響及びダルナビルが併用薬の薬物動態に及ぼす影響について表8、9に示す。[10.1、10.2 参照]
| 併用薬 | 併用薬の 用法及び用量 |
ダルナビルの 用法及び用量 |
リトナビルの 用法及び用量 |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | |||||
| エファビレンツ | 600mg 1日1回 |
300mg 1日2回 |
100mg 1日2回 |
12 | 0.85 [0.72, 1.00] |
0.87 [0.75, 1.01] |
0.69 [0.54, 0.87] |
| ネビラピン | 200mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
8 | 1.40 [1.14, 1.73] |
1.23 [0.97, 1.57] |
1.02 [0.79, 1.32] |
| セルトラリン | 50mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
13 | 1.01 [0.89, 1.14] |
0.98 [0.84, 1.14] |
0.94 [0.76, 1.16] |
| パロキセチン | 20mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
16 | 0.97 [0.92, 1.02] |
1.02 [0.95, 1.10] |
1.07 [0.96, 1.19] |
| ラニチジン | 150mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
16 | 0.96 [0.89, 1.05] |
0.95 [0.90, 1.01] |
0.94 [0.90, 0.99] |
| オメプラゾール | 20mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
16 | 1.02 [0.95, 1.09] |
1.04 [0.96, 1.13] |
1.08 [0.93, 1.25] |
| ジダノシン | 400mg 1日1回 |
600mg 1日2回 |
100mg 1日2回 |
17 | 0.93 [0.86, 1.00] |
1.01 [0.95, 1.07] |
1.07 [0.95, 1.21] |
| テノホビル ジソプロキシルフマル酸塩 | 300mg 1日1回 |
300mg 1日2回 |
100mg 1日2回 |
12 | 1.16 [0.94, 1.42] |
1.21 [0.95, 1.54] |
1.24 [0.90, 1.69] |
| ケトコナゾール | 200mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
14 | 1.21 [1.04, 1.40] |
1.42 [1.23, 1.65] |
1.73 [1.39, 2.14] |
| クラリスロマイシン | 500mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
17 | 0.83 [0.72, 0.96] |
0.87 [0.75, 1.01] |
1.01 [0.81, 1.26] |
| リファブチン | 150mg 隔日1回 |
600mg 1日2回 |
100mg 1日2回 |
11注1) | 1.42 [1.21, 1.67] |
1.57 [1.28, 1.93] |
1.75 [1.28, 2.37] |
| カルバマゼピン | 200mg 1日2回 |
600mg 1日2回 |
100mg 1日2回 |
11注1) | 1.04 [0.93, 1.16] |
0.99 [0.90, 1.08] |
0.85 [0.73, 1.00] |
| リルピビリン | 150mg 1日1回 |
800mg 1日1回 |
100mg 1日1回 |
14注2) | 0.90 [0.81, 1.00] |
0.89 [0.81, 0.99] |
0.89 [0.68, 1.16] |
| エトラビリン | 200mg 1日2回 |
600mg 1日2回 |
100mg 1日2回 |
10注2) | 1.11 [1.01, 1.22] |
1.15 [1.05, 1.26] |
1.02 [0.90, 1.17] |
| アルテメテル・ルメファントリン配合剤 | アルテメテル・ルメファントリン配合剤 80・480mg,3日間投与 (0,8,24,36,48及び 60時間に投与) |
600mg 1日2回 |
100mg 1日2回 |
14 | 1.00 [0.93, 1.07] |
0.96 [0.90, 1.03] |
0.87 [0.77, 0.98] |
| ロピナビル | ロピナビル・リトナビル配合剤 400・100mg 1日2回 |
300mg 1日2回 |
100mg 1日2回 |
9 | 0.61 [0.51, 0.74] |
0.47 [0.40, 0.55] |
0.35 [0.29, 0.42] |
| NA | 8 | 0.67 [0.53, 0.84] |
0.47 [0.37, 0.59] |
0.36 [0.29, 0.46] |
|||
| インジナビル | 800mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
9 | 1.11 [0.98, 1.26] |
1.24 [1.09, 1.42] |
1.44 [1.13, 1.82] |
| アタザナビル | 300mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
13 | 1.02 [0.96, 1.09] |
1.03 [0.94, 1.12] |
1.01 [0.88, 1.16] |
NA:未投与
注1)非併用投与時:16例
注2)非併用投与時:15例
| 併用薬 | 併用薬の |
ダルナビルの |
リトナビルの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | |||||
| エファビレンツ | 600mg 1日1回 |
300mg 1日2回 |
100mg 1日2回 |
12 | 1.15 [0.97, 1.35] |
1.21 [1.08, 1.36] |
1.17 [1.01, 1.36] |
| ネビラピン | 200mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
8 | 1.18 [1.02, 1.37] |
1.27 [1.12, 1.44] |
1.47 [1.20, 1.82] |
| プラバスタチン | 40mg 単回 |
600mg 1日2回 |
100mg 1日2回 |
14 | 1.63 [0.95, 2.82] |
1.81 [1.23, 2.66] |
NC |
| セルトラリン | 50mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
13 | 0.56 [0.49, 0.63] |
0.51 [0.46, 0.58] |
0.51 [0.45, 0.57] |
| パロキセチン | 20mg 1日1回 |
400mg 1日2回 |
100mg 1日2回 |
16 | 0.64 [0.59, 0.71] |
0.61 [0.56, 0.66] |
0.63 [0.55, 0.73] |
| ジダノシン | 400mg 1日1回 |
600mg 1日2回 |
100mg 1日2回 |
17 | 0.84 [0.59, 1.20] |
0.91 [0.75, 1.10] |
NC |
| テノホビル ジソプロキシルフマル酸塩 | 300mg 1日1回 |
300mg 1日2回 |
100mg 1日2回 |
12 | 1.24 [1.08, 1.42] |
1.22 [1.10, 1.35] |
1.37注1) [1.19, 1.57] |
| R(-)メサドン | メサドン 55~150mg 1日1回 |
600mg 1日2回 |
100mg 1日2回 |
16 | 0.76 [0.71, 0.81] |
0.84 [0.78, 0.91] |
0.85 [0.77, 0.94] |
| S(+)メサドン | 0.56 [0.51, 0.62] |
0.64 [0.58, 0.71] |
0.60 [0.53, 0.69] |
||||
| シルデナフィル | シルデナフィル 25mg単回注2)/ 100mg単回注3) |
400mg 1日2回 |
100mg 1日2回 |
16 | 0.62 [0.55, 0.70] |
0.97 [0.86, 1.09] |
NC |
| N-デスメチルシルデナフィル | 0.05 [0.04, 0.05] |
0.05 [0.04, 0.08] |
NC | ||||
| ケトコナゾール | 200mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
15 | 2.11 [1.81, 2.44] |
3.12 [2.65, 3.68] |
9.68 [6.44, 14.55] |
| エチニルエストラジオール | エチニルエストラジオール・ ノルエチステロン配合剤 (各35μg・1.0mg含有) 1日1回 |
600mg 1日2回 |
100mg 1日2回 |
11注4) | 0.68 [0.61, 0.74] |
0.56 [0.50, 0.63] |
0.38 [0.27, 0.54] |
| ノルエチステロン | 0.90 [0.83, 0.97] |
0.86 [0.75, 0.98] |
0.70 [0.51, 0.97] |
||||
| アトルバスタチン | アトルバスタチン 1日1回注2)/ 40mg1日1回注3) |
300mg 1日2回 |
100mg 1日2回 |
15 | 0.56 [0.48, 0.67] |
0.85 [0.76, 0.97] |
1.81 [1.37, 2.40] |
| アトルバスタチンラクトン | 0.85 [0.76, 0.96] |
1.07 [0.96, 1.19] |
2.08 [1.63, 2.65] |
||||
| クラリスロマイシン | 500mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
17 | 1.26 [1.03, 1.54] |
1.57 [1.35, 1.84] |
2.74 [2.30, 3.26] |
| ジゴキシン | 0.4mg 単回 |
600mg 1日2回 |
100mg 1日2回 |
8 | 1.15 [0.89, 1.48] |
1.36 [0.81, 2.26] |
NC |
| リファブチン | リファブチン 隔日1回注2)/ 300mg1日1回注3) |
600mg 1日2回 |
100mg 1日2回 |
11注5) | 0.72 [0.55, 0.93] |
0.93 [0.80, 1.09] |
1.64 [1.48, 1.81] |
| 25-脱アセチル体代謝物 | 4.77 [4.04, 5.63] |
9.81 [8.09, 11.9] |
27.1 [22.15, 33.16] |
||||
| ブプレノルフィン | ブプレノルフィン・ナロキソン配合剤 1日1回最大 16・4mg |
600mg 1日2回 |
100mg 1日2回 |
17 | 0.92 [0.79, 1.08] |
0.89 [0.78, 1.02] |
0.98 [0.82, 1.16] |
| ノルブプレノルフィン | 17 | 1.36 [1.06, 1.74] |
1.46 [1.15, 1.85] |
1.71 [1.29, 2.27] |
|||
| カルバマゼピン | 200mg 1日2回 |
600mg 1日2回 |
100mg 1日2回 |
16 | 1.43 [1.34, 1.53] |
1.45 [1.35, 1.57] |
1.54 [1.41, 1.68] |
| カルバマゼピンエポキシド | 16 | 0.46 [0.43, 0.49] |
0.46 [0.44, 0.49] |
0.48 [0.45, 0.51] |
|||
| ラルテグラビル | 400mg 1日2回 |
600mg 1日2回 |
100mg 1日2回 |
6 | 0.67注6) [0.33, 1.37] |
0.71注6) [0.38, 1.33] |
NC |
| マラビロク | 150mg 1日2回 |
600mg 1日2回 |
100mg 1日2回 |
12 | 2.29注6) [1.46, 3.59] |
4.05注6) [2.94, 5.59] |
8.00 [6.35, 10.1] |
| リルピビリン | 150mg 1日1回 |
800mg 1日1回 |
100mg 1日1回 |
14 | 1.79 [1.56, 2.06] |
2.30 [1.98, 2.67] |
2.78 [2.39, 3.24] |
| エトラビリン | 200mg 1日2回注2)/ 100mg 1日2回注3) |
600mg 1日2回 |
100mg 1日2回 |
10注7) | 1.81 [1.56, 2.11] |
1.80 [1.56, 2.08] |
1.67 [1.38, 2.03] |
| アルテメテル | アルテメテル・ルメファントリン配合剤 80・480mg,3日間投与 (0,8,24,36,48及び 60時間に投与) |
600mg 1日2回 |
100mg 1日2回 |
14注5) | 0.82 [0.61, 1.11] |
0.84 [0.69, 1.02] |
0.97 [0.90, 1.05] |
| ジヒドロアルテミシニン | 0.82 [0.66, 1.01] |
0.82 [0.74, 0.91] |
1.00 [0.82, 1.22] |
||||
| ルメファントリン | 1.65 [1.49, 1.83] |
2.75 [2.46, 3.08] |
2.26注8) [1.92, 2.67] |
||||
| ロピナビル | ロピナビル・リトナビル配合剤 400・100mg 1日2回 |
300mg 1日2回 |
100mg 1日2回 |
9 | 1.22 [1.12, 1.32] |
1.37 [1.27, 1.49] |
1.72 [1.46, 2.03] |
| NA | 8 | 0.83 [0.70, 0.99] |
0.81 [0.70, 0.94] |
0.65 [0.48, 0.88] |
|||
| インジナビル | 800mg 1日2回 |
400mg 1日2回 |
100mg 1日2回 |
9 | 1.08 [0.95, 1.22] |
1.23 [1.06, 1.42] |
2.25 [1.63, 3.10] |
| S-ワルファリン | ワルファリン 10mg+ビタミンK1 10mg+ デキストロメトルファン 30mg+ オメプラゾール 40mg 単回 |
600mg 1日2回 |
100mg 1日2回 |
12 | 0.92 [0.86, 0.98] |
0.79 [0.74, 0.86] |
NC |
| 7-OH-S-ワルファリン | 12 | 1.43 [1.24, 1.64] |
1.24 [0.97, 1.58] |
NC | |||
| デキストロメトルファン | 12 | 2.27 [1.59, 3.26] |
2.70 [1.80, 4.05] |
NC | |||
| デキストルファン | 12 | 0.87 [0.77, 0.98] |
0.96 [0.90, 1.03] |
NC | |||
| オメプラゾール | 12 | 0.66 [0.48, 0.91] |
0.58 [0.51, 0.67] |
NC | |||
| 5-OH-オメプラゾール | 12 | 0.94 [0.72, 1.22] |
0.85 [0.77, 0.93] |
NC | |||
**(3)コビシスタット
併用薬がコビシスタットの薬物動態に及ぼす影響及びコビシスタットが併用薬の薬物動態に及ぼす影響について表10、11に示す。[10.2 参照]
| 併用薬 | 併用薬の |
コビシスタットの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Ctau | ||||
| ファモチジン | 40mg 1日1回 夜,食後, エルビテグラビル, コビシスタット投与後12時間後 |
150mg 1日1回, 朝,食後 |
10 | 1.04 [0.99, 1.08] |
1.05 [1.02, 1.08] |
1.15 [1.06, 1.26] |
| 40mg 1日1回 朝,食後 |
16 | 1.06 [0.99, 1.13] |
1.03 [0.97, 1.11] |
1.11 [1.00, 1.24] |
||
| オメプラゾール | 20mg 1日1回, 朝,絶食下 |
11 | 0.90 [0.82, 0.99] |
0.92 [0.85, 1.01] |
0.93 [0.74, 1.17] |
|
| 20mg 1日1回, 夜,絶食下, エルビテグラビル, コビシスタット投与後12時間後 |
11 | 0.94 [0.85, 1.05] |
0.99 [0.89, 1.09] |
1.02注2) [0.82, 1.28] |
||
注1)エルビテグラビル150mg1日1回との併用投与
注2)10例
| 併用薬 | 併用薬の |
コビシスタットの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Ctau | ||||
| デシプラミン (国内未承認) |
50mg 単回 |
150mg 1日1回 |
8 | 1.24 [1.08, 1.44] |
1.58 [1.35, 1.84] |
NC |
| ジゴキシン | 0.5mg 単回 |
22 | 1.41 [1.29, 1.55] |
1.20 [1.10, 1.30] |
NC | |
| エファビレンツ | 600mg 単回 |
17 | 0.87 [0.80, 0.94] |
0.93 [0.90, 0.96] |
NC | |
| ロスバスタチン | 10mg 単回 |
150mg 1日1回 |
10 | 1.89 [1.48, 2.42] |
1.38 [1.14, 1.67] |
1.43 [1.08, 1.89]注2) |
| リファブチン | リファブチン 150mg 隔日1回注3)/ 300mg1日1回注4) |
150mg 1日1回 |
12 | 1.09 [0.98, 1.20] |
0.92 [0.83, 1.03] |
0.94 [0.85, 1.04] |
| 25-脱アセチル体代謝物 | 4.84 [4.09, 5.74] |
6.25 [5.08, 7.69] |
4.94 [4.04, 6.04] |
|||
| ノルゲスチメート及び エチニルエストラジオール |
0.180/0.215/0.250mg ノルゲスチメート 1日1回 |
150mg 1日1回注5) |
15 | 2.08 [2.00, 2.17] |
2.26 [2.15, 2.37] |
2.67 [2.43, 2.92] |
| 0.025mg エチニルエストラジオール 1日1回 |
0.94 [0.86, 1.04] |
0.75 [0.69, 0.81] |
0.56 [0.52, 0.61] |
|||
| ブプレノルフィン | ブプレノルフィン 16~24mg 1日1回 |
150mg 1日1回 |
17 | 1.12 [0.98, 1.27] |
1.35 [1.18, 1.55] |
1.66 [1.31, 1.93] |
| ノルブプレノルフィン | 1.24 [1.03, 1.49] |
1.42 [1.22, 1.67] |
1.57 [1.31, 1.88] |
|||
| R-メサドン | メサドン 80~120mg 1日1回 |
150mg 1日1回 |
11 | 1.01 [0.91, 1.13] |
1.07 [0.96, 1.19] |
1.10 [0.95, 1.28] |
| S-メサドン | 0.96 [0.87, 1.06] |
1.00 [0.89, 1.12] |
1.02 [0.89, 1.17] |
|||
| ナロキソン | 4~6mg 1日1回 |
150mg 1日1回 |
17 | 0.72 [0.61, 0.85] |
0.72 [0.59, 0.87] |
NC |
(4)エムトリシタビン
併用薬がエムトリシタビンの薬物動態に及ぼす影響及びエムトリシタビンが併用薬の薬物動態に及ぼす影響について表12、13に示す。[10.2 参照]
| 併用薬 | 併用薬の |
エムトリシタビンの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| ダルナビル | 800mg +コビシスタット150mg 1日1回 |
200mg 1日1回注1) |
11 | 1.13 [1.02, 1.24] |
1.24 [1.17, 1.31] |
1.31 [1.24, 1.38] |
| エファビレンツ | 600mg 1日1回 |
200mg 1日1回 |
11 | 0.90 [0.81, 0.99] |
0.92 [0.87, 0.96] |
0.92 [0.86, 0.98] |
| セルトラリン | 50mg 単回 |
200mg 1日1回注2) |
19 | 0.90 [0.82, 0.98] |
0.84 [0.81, 0.88] |
0.94 [0.90, 0.99] |
| タクロリムス | 0.05mg/kg 1日2回 |
200mg 1日1回注3) |
21 | 0.89 [0.83, 0.95] |
0.95 [0.91, 0.99] |
1.03 [0.96, 1.10] |
| ファムシクロビル | 500mg 単回 |
200mg 単回 |
12 | 0.90 [0.80, 1.01] |
0.93 [0.87, 0.99] |
NC |
| テノホビル ジソプロキシルフマル酸塩 | 300mg 1日1回 7日間 |
200mg 1日1回 7日間 |
17 | 0.96 [0.87, 1.06] |
1.07 [1.00, 1.14] |
1.20 [1.12, 1.29] |
| インジナビル | 800mg 単回 |
200mg 単回 |
12 | 0.92 [0.82, 1.04] |
1.01 [0.94, 1.09] |
NC |
| サニルブジン | 40mg 単回 |
200mg 単回 |
6 | 1.04 [0.94, 1.16] |
1.02 [0.94, 1.11] |
NC |
| ジドブジン | 300mg 1日2回 7日間 |
200mg 1日1回 7日間 |
27 | 0.97 [0.90, 1.04] |
0.97 [0.93, 1.01] |
0.96 [0.88, 1.04] |
| ソホスブビル・ベルパタスビル配合剤 | 400・100mg 1日1回 |
200mg 1日1回注2) |
24 | 1.02 [0.97, 1.06] |
1.01 [0.98, 1.04] |
1.02 [0.97, 1.07] |
NC:未算出
注1)エムトリシタビン・テノホビル アラフェナミド配合剤を用いた薬物動態試験
注2)エルビテグラビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド(10mg)配合剤を用いた薬物動態試験
注3)エムトリシタビン・テノホビル ジソプロキシルフマル酸塩配合剤を用いた薬物動態試験
| 併用薬 | 併用薬の |
エムトリシタビンの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| テノホビル ジソプロキシルフマル酸塩 | 300mg 1日1回 7日間 |
200mg 1日1回 7日間 |
17 | 1.03 [0.95, 1.11] |
1.00 [0.92, 1.09] |
1.02 [0.92, 1.13] |
| インジナビル | 800mg 単回 |
200mg 単回 |
12 | 0.98 [0.84, 1.13] |
1.02 [0.89, 1.17] |
NC |
| サニルブジン | 40mg 単回 |
200mg 単回 |
6 | 1.05 [0.95, 1.16] |
1.09 [0.83, 1.44] |
NC |
| ジドブジン | 300mg 1日2回 7日間 |
200mg 1日1回 7日間 |
27 | 1.17 [1.00, 1.38] |
1.13 [1.05, 1.20] |
0.98 [0.89, 1.09] |
NC:未算出
(5)テノホビル アラフェナミド
併用薬がテノホビル アラフェナミドの薬物動態に及ぼす影響及びテノホビル アラフェナミドが併用薬の薬物動態に及ぼす影響について表14、15に示す。[10.1、10.2 参照]
| 併用薬 | 併用薬の |
テノホビル アラフェナミドの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| カルバマゼピン | 300mg 1日2回 |
25mg 単回 |
26 | 0.43 [0.36, 0.51] |
0.45 [0.40, 0.51] |
NC |
| アタザナビル | 300mg +リトナビル 100mg 1日1回 |
10mg 単回 |
10 | 1.77 [1.28, 2.44] |
1.91 [1.55, 2.35] |
NC |
| コビシスタット | 150mg 1日1回 |
8mg 1日1回 |
12 | 2.83 [2.20, 3.65] |
2.65 [2.29, 3.07] |
NC |
| ダルナビル | 800mg +コビシスタット150mg 1日1回 |
25mg 1日1回注1) |
11 | 0.93 [0.72, 1.21] |
0.98 [0.80, 1.19] |
NC |
| 800mg +リトナビル 100mg 1日1回 |
10mg 単回 |
10 | 1.42 [0.96, 2.09] |
1.06 [0.84, 1.35] |
NC | |
| ドルテグラビル | 50mg 1日1回 |
10mg 単回 |
10 | 1.24 [0.88, 1.74] |
1.19 [0.96, 1.48] |
NC |
| エファビレンツ | 600mg 1日1回 |
40mg 1日1回 |
11 | 0.78 [0.58, 1.05] |
0.86 [0.2, 1.02] |
NC |
| ロピナビル・リトナビル配合剤 | 800mg +リトナビル 200mg 1日1回 |
10mg 単回 |
10 | 2.19 [1.72, 2.79] |
1.47 [1.17, 1.85] |
NC |
| セルトラリン | 50mg 単回 |
10mg 1日1回注2) |
19 | 1.00 [0.86, 1.16] |
0.96 [0.89, 1.03] |
NC |
| リルピビリン | 25mg 1日1回 |
25mg 1日1回 |
32 | 1.01 [0.84, 1.22] |
1.01 [0.94, 1.10] |
NC |
| ソホスブビル・ベルパタスビル配合剤 | 400・100mg 1日1回 |
10mg 1日1回注2) |
24 | 0.80 [0.68, 0.94] |
0.87 [0.81, 0.94] |
NC |
NC:未算出
注1)エムトリシタビン・テノホビル アラフェナミドフマル酸塩配合剤を用いた薬物動態試験
注2)エルビテグラビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド(10mg)配合剤を用いた薬物動態試験
| 併用薬 | 併用薬の |
テノホビル アラフェナミドの |
例数 | 他剤併用時/非併用時の 薬物動態パラメータの比 [90%信頼区間] |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| カルバマゼピン | 300mg 1日2回 |
25mg 単回 |
26 | 0.70 [0.65, 0.74] |
0.77 [0.74, 0.81] |
NC |
| アタザナビル | 300mg +リトナビル 100mg |
1日1回 10mg 単回 |
10 | 0.98 [0.89, 1.07] |
0.99 [0.96, 1.01] |
1.00 [0.96, 1.04] |
| コビシスタット | 150mg 1日1回 |
25mg 1日1回注1) |
14 | 1.06 [1.00, 1.12] |
1.09 [1.03, 1.15] |
1.11 [0.98, 1.25] |
| ダルナビル | 800mg +コビシスタット150mg 1日1回 |
25mg 1日1回注1) |
14 | 1.02 [0.96, 1.09] |
0.99 [0.92, 1.07] |
0.97 [0.82, 1.15] |
| 800mg +リトナビル 100mg 1日1回 |
10mg 単回 |
10 | 0.99 [0.91, 1.08] |
1.01 [0.96, 1.06] |
1.13 [0.95, 1.34] |
|
| ドルテグラビル | 50mg 1日1回 |
10mg 単回 |
10 | 0.87 [0.79, 0.96] |
0.98 [0.93, 1.03] |
0.95 [0.88, 1.03] |
| ロピナビル・リトナビル配合剤 | 800mg +リトナビル 200mg 1日1回 |
10mg 単回 |
10 | 1.00 [0.95, 1.06] |
1.00 [0.92, 1.09] |
0.98 [0.85, 1.12] |
| ミダゾラム | 2.5mg 単回経口 |
25mg 1日1回 |
18 | 1.02 [0.92, 1.13] |
1.12 [1.03, 1.22] |
NC |
| 1mg 単回静脈内 |
25mg 1日1回 |
18 | 0.99 [0.89, 1.11] |
1.08 [1.04, 1.14] |
NC | |
| セルトラリン | 50mg 単回 |
10mg 1日1回注2) |
20 | 1.14 [0.94, 1.38] |
1.09 [0.90,1.32] |
NC |
| リルピビリン | 25mg 1日1回 |
25mg 1日1回 |
32 | 0.93 [0.87, 0.99] |
1.01 [0.96, 1.06] |
1.13 [1.04, 1.23] |
| ベルパタスビル | ベルパタスビル100mg +ソホスブビル +400mg 1日1回 |
10mg 1日1回注2) |
24 | 1.30 [1.17, 1.45] |
1.50 [1.35, 1.66] |
1.60 [1.44, 1.78] |
| ソホスブビル | 1.23 [1.07, 1.42] |
1.37 [1.24, 1.52] |
NC | |||
| ソホスブビルの主代謝物 | 1.29 [1.25, 1.33] |
1.48 [1.43, 1.53] |
1.58 [1.52, 1.65] |
|||
NC:未算出
注1)エムトリシタビン・テノホビル アラフェナミドフマル酸塩配合剤を用いた薬物動態試験
注2)エルビテグラビル・コビシスタット・テノホビル アラフェナミド(10mg)・エムトリシタビン配合剤を用いた薬物動態試験
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 海外第III相試験(TMC114FD2HTX3001試験(AMBER試験))
抗HIV薬治療未経験のHIV-1感染患者を対象に、本剤(本剤群)の有効性及び安全性を検討するため、ダルナビル・コビシスタット配合剤(DRV・COBI)とエムトリシタビン・テノホビル ジソプロキシルフマル酸塩配合剤(FTC・TDF)の併用(DRV・COBI、FTC・TDF併用群)を対照としたランダム化二重盲検並行群間比較試験を実施した。48週時の臨床成績を表1に示す。
FDAのsnapshotアプローチに基づく48週時のウイルス学的効果(HIV-1 RNA量が50copies/mL未満に維持されていた患者の割合)を主要評価項目とし、DRV・COBI、FTC・TDF併用群に対する本剤群の非劣性が検証された[群間差(95%CI):2.7(-1.6〜7.1)%]。33)[5.2、18.3.2 参照]
| 本剤群 362例 |
DRV・COBI、 363例 |
|
|---|---|---|
| ウイルス学的効果 HIV RNA量<50copies/mL |
331(91.4%) | 321(88.4%) |
| ウイルス学的治療失敗注1) | 16(4.4%) | 12(3.3%) |
注1)48週時にHIV RNA量が50copies/mL以上の患者、有効性の欠如又は消失のために試験を中止した患者、有害事象、死亡及び有効性の欠如又は消失以外の理由で試験を中止し中止時点のウイルス量が50copies/mL以上であった患者を含む。
副作用は362例中182例(50.3%)に認められた。主な副作用は、下痢71例(19.6%)、頭痛47例(13.0%)、発疹44例(12.2%)、悪心28例(7.7%)、疲労19例(5.2%)であった。
17.1.2 海外第III相試験(TMC114IFD3013試験(EMERALD試験))
プロテアーゼ阻害剤、薬物動態学的増強因子(ブースター)及びFTC・TDF配合剤の併用投与によりウイルス学的抑制が得られているHIV-1感染患者を対象に、本剤1日1回投与に切り替えた際の有効性及び安全性を評価するためのランダム化非盲検並行群間比較試験を実施した。48週時の臨床成績を表2に示す。
治験実施計画書の規定に基づく48週時までのウイルス学的リバウンド(HIV-1 RNA量が50copies/mL以上となった患者の割合)を主要評価項目とし、治療継続群に対する本剤群の非劣性が検証された[群間差(95%CI):0.4(-1.5~2.2)%]。34)[5.2、18.3.2 参照]
| 本剤群 763例 |
治療継続群 378例 |
|
|---|---|---|
| ウイルス学的リバウンド注1) HIV RNA量≥50copies/mL |
19(2.5%) | 8(2.1%) |
| ウイルス学的効果注2) HIV RNA量<50copies/mL |
724(94.9%) | 354(93.7%) |
注1)48週時までにHIV RNA量が50copies/mL以上の患者、及び理由を問わず試験を早期に中止し、中止時点のウイルス量が50copies/mL以上であった患者
注2)FDAのsnapshotアプローチに基づくウイルス学的効果
副作用は763例中236例(30.9%)に認められた。主な副作用は、下痢60例(7.9%)、頭痛58例(7.6%)、腹痛41例(5.4%)、発疹28例(3.7%)、嘔吐22例(2.9%)であった。
18. 薬効薬理
18.1 作用機序
18.1.1 ダルナビル
ダルナビルはHIV-1プロテアーゼの2量体化及び酵素活性を阻害する。本剤はHIV-1感染細胞においてウイルスのコードするGag-Polポリタンパク質の切断を選択的に阻害し、その結果、感染性を有する成熟ウイルスの形成を抑制する。本剤はHIV-1プロテアーゼに強い親和性(KD4.5×10-12mol/L)を有しており、HIVプロテアーゼ阻害剤耐性関連変異の影響も受けにくかった。他の代表的な13種のヒトプロテアーゼに対する阻害作用は認められなかった。35)~39)
18.1.2 コビシスタット
コビシスタットは、CYP3Aの選択的な阻害薬である。CYP3Aによる代謝によって吸収率の低下及び半減期の短縮が認められるダルナビル等のCYP3A基質に対し、CYP3Aを阻害することによって体内曝露を増加させる。
18.1.3 エムトリシタビン
エムトリシタビン(FTC)は、シチジンの合成ヌクレオシド誘導体であり、細胞内酵素によりリン酸化されエムトリシタビン5’-三リン酸となる。エムトリシタビン5’-三リン酸はHIV-1 RTによりウイルスDNAへ取り込まれた後、DNA鎖伸長を停止させることによりHIV-1ウイルスの複製を阻害する。FTCはヒトHIV(HIV-1及びHIV-2)並びにB型肝炎ウイルスに対して特異的に作用する。ミトコンドリアDNAポリメラーゼγを含む哺乳類のDNAポリメラーゼに対するエムトリシタビン5’-三リン酸の阻害作用は弱く、in vitro及びin vivoにおけるミトコンドリア障害を示す結果は得られていない。
18.1.4 テノホビル アラフェナミド
テノホビル アラフェナミド(TAF)は、テノホビルのホスホンアミド酸プロドラッグ(2’-デオキシアデノシン一リン酸誘導体)である。TAFは細胞内透過性を有し、血漿中の安定性が高く、カテプシンAにより加水分解を受けて細胞内で活性化される。そのため、テノホビル ジソプロキシルフマル酸塩(TDF)と比べ、TAFはリンパ球及びHIVが標的とするリンパ球以外の末梢血単核球、並びにマクロファージへより効率的に送達する。その後、細胞内でリン酸化を受け、活性代謝物のテノホビル二リン酸となる。テノホビル二リン酸は、HIV RTによりウイルスDNAに取り込まれた後、DNA鎖伸長を停止させることにより、HIVの複製を阻害する。
テノホビルはヒトHIVウイルス(HIV-1及びHIV-2)、並びにB型肝炎ウイルスに特異的に作用する。In vitro試験では、FTCとテノホビルを併用すると細胞内で完全にリン酸化される。
ミトコンドリアDNAポリメラーゼγを含む哺乳類のDNAポリメラーゼに対するテノホビル二リン酸の阻害作用は弱い。ミトコンドリアDNA分析を含む複数の評価から、in vitroでミトコンドリア障害を示す結果は得られていない。
18.2 抗ウイルス作用
18.2.1 ダルナビル
ダルナビルはヒトT細胞株、ヒト末梢血単核球及びヒト単球/マクロファージに急性感染させたHIV-1実験室株及び臨床分離株、並びにHIV-2実験室株に対し抑制作用(EC50値:1.2~8.5nmol/L)を示す。ダルナビルはHIV-1グループM(A、B、C、D、E、F、G)及びグループOの臨床分離株群及び初代分離株群にin vitroで抗ウイルス活性(EC50値:<0.1~4.3nmol/L)を示す。In vitroにおけるダルナビルの抗ウイルス作用は、50%細胞毒性作用を示す濃度(87~>100μmol/L)よりも十分に低い濃度で認められる。ダルナビルのEC50値はヒト血清存在下では中央値で5.4倍高い。ダルナビルはHIVプロテアーゼ阻害剤(アンプレナビル、ネルフィナビル及びリトナビル)と併用することにより相乗作用を示し、NRTI(アバカビル、ジダノシン、FTC、ラミブジン、サニルブジン、テノホビル及びジドブジン)、NNRTI(エトラビリン、エファビレンツ、ネビラピン及びリルピビリン)、HIVプロテアーゼ阻害剤(アタザナビル、インジナビル、ロピナビル、サキナビル及びtipranavir)及び融合阻害剤(enfuvirtide)と併用することにより相加作用を示した。ダルナビルとこれらの薬剤との併用において拮抗作用は認められなかった。40)~44)
18.2.2 コビシスタット
コビシスタットは、HIV-1に対する抗ウイルス活性を有さず、ダルナビル、FTC及びTAFの抗ウイルス活性に対する拮抗作用は認められなかった。
18.2.3 エムトリシタビン
ヒトリンパ芽球様細胞株、MAGI-CCR5細胞株及び末梢血単核球を用いて、HIV-1の実験室株及び臨床分離株に対するFTCの抗ウイルス活性を評価した。FTCのEC50値は、0.0013~0.64μmol/Lの範囲であった。FTCは、培養細胞系においてHIV-1のサブタイプA、B、C、D、E、F及びGに対して抗ウイルス活性を示し(EC50値:0.007~0.075μmol/L)、HIV-2に対して株特異的な抗ウイルス活性を示した(EC50値:0.007~1.5μmol/L)。
FTCは、NRTI(アバカビル、ジダノシン、ラミブジン、サニルブジン、テノホビル及びジドブジン)、NNRTI(エファビレンツ、ネビラピン及びリルピビリン)、プロテアーゼ阻害剤(アンプレナビル、ネルフィナビル、リトナビル及びサキナビル)、並びにインテグラーゼ阻害剤のエルビテグラビルとの2剤併用試験において、相加又は相乗効果を示した。これらの薬剤との併用では拮抗作用はみられなかった。
18.2.4 テノホビル アラフェナミド
リンパ芽球様細胞株、末梢血単核球、初代培養単球/マクロファージ及びCD4陽性Tリンパ球を用いて、HIV-1サブタイプBの実験室株及び臨床分離株に対するTAFの抗ウイルス活性を評価した。TAFのEC50値は、2.0〜14.7nmol/Lの範囲であった。
TAFは、培養細胞系においてサブタイプA、B、C、D、E、F及びGを含むHIV-1のすべてのグループ(M、N、O)に対して抗ウイルス活性を示し(EC50値:0.10~12.0nmol/L)、HIV-2に対して株特異的な抗ウイルス活性を示した(EC50値:0.91~2.63nmol/L)。
TAFは、主要なクラスの代表的な既承認抗HIV薬(NRTI、NNRTI、インテグラーゼ阻害剤及びプロテアーゼ阻害剤)との併用により相加又は相乗効果を示した。これらの薬剤との併用では拮抗作用はみられなかった。
18.3 薬剤耐性
18.3.1 In vitro試験
(1)ダルナビル
ダルナビル存在下で培養した野生型HIV-1から耐性ウイルスを得るために、3年以上の継代を繰り返したところ、耐性ウイルスの発現が認められた。耐性ウイルスに対してダルナビルは400nmol/Lを超える濃度で増殖抑制を示した(in vitro)。この耐性ウイルスは、ダルナビルに対しての感受性が23~50倍低下しており、プロテアーゼ遺伝子に2~4個のアミノ酸置換を有していた。これらのウイルスのダルナビル耐性因子とプロテアーゼ内のアミノ酸変異の関連性は認められなかった。HIVプロテアーゼ阻害剤耐性変異を有する9株のHIV-1からダルナビルの耐性株(EC50値が53~641倍変化)をin vitroで獲得した結果、ダルナビル耐性株のプロテアーゼ内に22個のアミノ酸変異が出現し、このうちL10F、V32I、L33F、S37N、M46I、I47V、I50V、L63P、A71V及びI84Vの変異は耐性分離株の50%超に認められた。ダルナビル耐性(EC50値の比;fold change[FC]>10)となるには、これらの変異のうち最低8個のHIVプロテアーゼ阻害剤耐性関連変異が必要であり、うち2個の変異はすでにプロテアーゼ遺伝子内に存在していた。アンプレナビル、アタザナビル、インジナビル、ロピナビル、ネルフィナビル、リトナビル、サキナビルあるいはtipranavirに耐性の臨床分離株1,113株、並びに海外臨床試験C202/C213試験及びC208/C215試験解析に組み入れられた被験者のダルナビル投与開始前の分離株886株において、ダルナビルに対するFC>10(中央値)を示したのは、10個を超えるHIVプロテアーゼ阻害剤耐性関連変異を持ったサブグループのみであった。
ダルナビル耐性関連変異(V11I、V32I、L33F、I47V、I50V、I54L/M、T74P、L76V、I84V 及びL89V)は、抗ウイルス剤の使用経験のある患者の臨床試験データから得られた。45)~47)
(2)エムトリシタビン
In vitroにおいて、FTC耐性HIV-1株を得た。FTCに対する感受性の低下と、HIV-1 RTのM184V/I変異との間に関連性が認められた。
(3)テノホビル アラフェナミド
TAFに対する感受性が低下したHIV-1分離株では、HIV-1 RTにK65R変異が発現しており、K70E変異も一過性に認められた。K65R変異を有するHIV-1分離株はアバカビル、FTC、テノホビル及びラミブジンに対する感受性が低下した。In vitro耐性獲得試験において、長期の培養後もTAFに対する高度な耐性株は出現しなかった。
18.3.2 臨床試験
プロテアーゼ阻害剤及びFTC・TDF配合剤の併用投与によりウイルス学的抑制が得られている患者を対象とした本剤の臨床試験(TMC114IFD3013試験)において、過去に治療失敗の経験がある169例のベースライン時検体を用いて遺伝子型解析を事後的に行い結果が得られた140例(本剤群98例、治療継続群42例)のうち、テノホビル耐性関連変異は4%(5/140例:本剤群 4/98例、治療継続群1/42例)に認められ、K65Rの変異が4例(本剤群4例)、K70位の変異が1例(治療継続群1例)に認められた。FTC耐性関連変異は38%(53/140例:本剤群35/98例、治療継続群18/42例)に認められ、M184位の変異が49例(本剤群31例、治療継続群18例)、K65Rの変異が4例(本剤群4例)に認められた。DRV耐性関連変異は4%(6/140例:本剤群4/98例、治療継続群2/42例)に認められ、I84V 4例(本剤群4例)、L33F 1例(治療継続群1例)、T74P 1例(治療継続群1例)及びL76V 1例(本剤群1例)に認められた。テノホビル、FTC及びDRV耐性関連変異が認められたすべての患者において、投与後48週時又は治療終了時点でHIV-1 RNA量<50copies/mLを達成した。ウイルス学的リバウンドが出現したすべての患者27例のうちベースライン時の遺伝子型解析結果が得られた24例においては、いずれもテノホビル、FTC又はDRV耐性関連変異は認められなかった。
抗HIV薬による治療未経験の患者を対象とした本剤の臨床試験(GS-US-299-0102試験、TMC114FD2HTX3001試験)及びTMC114IFD3013試験において、本剤が投与された1228例のうち、投与期間中にHIV-1 RNA量が400copies/mL以上等のウイルス学的リバウンド又は失敗の基準を満たし、本剤投与後の耐性検査が実施された14例では、NRTI関連耐性変異は3例に認められ、そのうちテノホビル又はFTC耐性関連変異は2例に認められ、M184I/V 2例(FTC耐性関連変異)、K65R 1例(テノホビル及びFTC耐性関連変異)が検出された。プロテアーゼ阻害剤の一次変異又はDRV耐性関連変異は認められなかった。[5.2、17.1.1、17.1.2 参照]
18.4 交叉耐性
18.4.1 ダルナビル
HIVプロテアーゼ阻害剤には交叉耐性が認められやすい。アンプレナビル、アタザナビル、インジナビル、ロピナビル、ネルフィナビル、リトナビル、サキナビル又はtipranavirに対する感受性が低下した臨床分離株3,309株の90%に対して、ダルナビルの感受性低下は10倍未満であり、ほとんどのHIVプロテアーゼ阻害剤に対して耐性を示すウイルスにダルナビルの感受性は保持されていた。作用機序の違いから、NRTI、NNRTI、融合阻害剤とダルナビルとの間に交叉耐性は生じないと考えられる。46)、47)
18.4.2 エムトリシタビン
FTC耐性株(M184V/I)はラミブジンに対して交叉耐性を示したが、ジダノシン、サニルブジン、テノホビル、ジドブジンに対しては感受性を維持した。サニルブジン及びジドブジンに対する感受性低下をもたらすチミジン誘導体関連変異(M41L、D67N、K70R、L210W、T215Y/F、K219Q/E)又はジダノシン関連変異(L74V)を有するウイルスは、FTCに対する感受性を維持した。NNRTI耐性と関連づけられるK103N変異又はその他の変異を有するHIV-1は、FTCに対して感受性を示した。
18.4.3 テノホビル アラフェナミド
K65R、K70E変異によりアバカビル、ジダノシン、ラミブジン、FTC、テノホビルに対する感受性が低下するが、ジドブジンに対する感受性は維持される。T69S二重挿入変異、又はK65Rを含むQ151M複合変異を持ち、核酸系逆転写酵素阻害薬に多剤耐性を持つHIV-1は、TAFに対する感受性の低下を示した。K103N又はY181CのNNRTI関連変異を有するHIV-1は、TAFに対して感受性を示した。プロテアーゼ関連変異を有するHIV-1はTAFに対して感受性を示した。
19. 有効成分に関する理化学的知見
19.1 ダルナビル エタノール付加物
| 一般的名称 | ダルナビル エタノール付加物(Darunavir Ethanolate) |
|---|---|
| 化学名 | (3R,3aS,6aR)-Hexahydrofuro[2,3-b]furan-3-yl[(1S,2R)-3-{[(4-aminophenyl)sulfonyl](2-methylpropyl)amino}-1-benzyl-2-hydroxypropyl]carbamate monoethanolate |
| 分子式 | C27H37N3O7S・C2H6O |
| 分子量 | 593.73 |
| 性状 | 白色の粉末 |
| 化学構造式 | 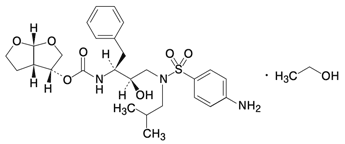 |
| 融点 | 100~105℃ |
| 分配係数 | Log P=2.47(1-オクタノール/pH7.0緩衝液) |
| 溶解性 | N,N-ジメチルホルムアミドに極めて溶けやすく、アセトニトリルに溶けやすく、メタノールにやや溶けにくく、エタノール(99.5)に溶けにくく、2-プロパノール及び水に極めて溶けにくい。 |
19.2 コビシスタット
| 一般的名称 | コビシスタット(Cobicistat) |
|---|---|
| 化学名 | 1,3-Thiazol-5-ylmethyl{(2R,5R)-5-[(2S)-2-(3-methyl-3-{[2-(1-methylethyl)-1,3-thiazol-4-yl]methyl}ureido)-4-(morpholin-4-yl)butanamido]-1,6-diphenylhexan-2-yl}carbamate |
| 分子式 | C40H53N7O5S2 |
| 分子量 | 776.02 |
| 性状 | 白色~微黄色の固体 |
| 化学構造式 | 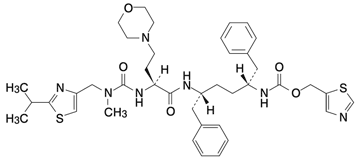 |
| 融点 | ガラス転移温度35℃、200℃以上(分解) |
| 分配係数 | Log P=4.3(1-オクタノール/pH8.5緩衝液) |
| 溶解性 | アセトニトリル、ジクロロメタン、ジメチルスルホキシド又はメタノールに溶けやすく、水又はヘプタンにほとんど溶けない。 |
19.3 エムトリシタビン
| 一般的名称 | エムトリシタビン(Emtricitabine) |
|---|---|
| 化学名 | 4-Amino-5-fluoro-1-[(2R,5S)-2-(hydroxymethyl)-1,3-oxathiolan-5-yl]pyrimidin-2(1H)-one |
| 分子式 | C8H10FN3O3S |
| 分子量 | 247.25 |
| 性状 | 白色~オフホワイトの粉末 |
| 化学構造式 |  |
| 融点 | 約155℃ |
| 分配係数 | Log P= -0.43(1-オクタノール/水) |
| 溶解性 | 水 112mg/mL アセトニトリル 4mg/mL 酢酸イソプロピル 0.3mg/mL |
19.4 テノホビル アラフェナミドフマル酸塩
| 一般的名称 | テノホビル アラフェナミドフマル酸塩(Tenofovir Alafenamide Fumarate) |
|---|---|
| 化学名 | 1-Methylethyl N-[(S)-{[(1R)-2-(6-amino-9H-purin-9-yl)-1-methylethoxy]methyl}phenoxyphosphinoyl]-L-alaninate hemifumarate |
| 分子式 | (C21H29N6O5P)2・C4H4O4 |
| 分子量 | 1069.00 |
| 性状 | 白色~灰白色又は白色~くすんだ黄赤色の粉末 |
| 化学構造式 | 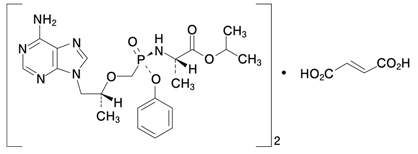 |
| 融点 | 約132℃ |
| 分配係数 | Log P=1.6(1-オクタノール/pH7のリン酸塩緩衝液) |
| 溶解性 | メタノール 189mg/mL エタノール 69.6mg/mL イソプロパノール 27.7mg/mL アセトン 9.16mg/mL アセトニトリル 2.30mg/mL トルエン 0.14mg/mL |
20. 取扱い上の注意
20.1
開栓後は、湿気を避けて保管すること。
20.2
小児の手の届かない所に保管すること。
**21. 承認条件
21.1
医薬品リスク管理計画を策定の上、適切に実施すること。
21.2
本剤の使用に当たっては、患者に対して本剤に関して更なる有効性・安全性のデータを引き続き収集中であること等を十分に説明し、インフォームドコンセントを得るよう、医師に要請すること。
21.3
海外において現在実施中又は計画中の臨床試験については、終了後速やかに試験成績及び解析結果を提出すること。
21.4
再審査期間が終了するまでの間、原則として国内の全投与症例を対象とした製造販売後調査を実施し、本剤の使用実態に関する情報(患者背景、有効性・安全性(他剤併用時の有効性・安全性を含む)及び薬物相互作用のデータ等)を収集して定期的に報告するとともに、調査の結果を再審査申請時に提出すること。
22. 包装
30錠[ボトル、バラ、乾燥剤入り]
23. 主要文献
- 社内資料:ダルナビルの乳汁移行試験(TMC114-NC249)
- 社内資料:コビシスタットの生殖発生毒性試験(TX-216-2033)
- Benaboud S, et al.:Antimicrob Agents Chemother. 2011;55:1315-1317
- 社内資料:ダルナビルの反復投与毒性試験(TMC114-NC130)
- 社内資料:ダルナビルの反復投与毒性試験(TMC114-NC132)
- 社内資料:ダルナビルとリトナビルの反復併用投与毒性試験(TMC114-NC146)
- 社内資料:ダルナビルのがん原性試験(TMC114-NC159)
- 社内資料:ダルナビルのがん原性試験(TMC114-NC158)
- **社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤の薬物動態に関する検討(TMC114FD2HTX4001)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤の薬物動態に関する検討(TMC114FD2HTX1001)(2019年6月18日承認、CTD2.7.1-2.2.1.1)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤の薬物動態に関する検討(GS-US-299-0101)(2019年6月18日承認、CTD2.7.1-2.1.1.2)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤の薬物動態に関する検討(GS-US-299-0102)(2019年6月18日承認、CTD2.7.2-2.2.2.1)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤の食事の影響及び薬物動態の検討(TMC114FD2HTX1002)(2019年6月18日承認、CTD2.7.1-2.1.1.1)
- 社内資料:ダルナビルの蛋白結合率の検討(TMC114-NC215(FK4948))
- 社内資料:コビシスタットの蛋白結合率の検討(GS-US-183-0133(60N-1103A))
- 社内資料:コビシスタットの蛋白結合率の検討(GS-US-216-0124(60N-1103B))
- 社内資料:ダルナビルの代謝の検討(TMC114-NC112(TNO41201))
- 社内資料:コビシスタットの薬物動態に関する検討(216-2025)
- 社内資料:コビシスタットの代謝の検討(AD-216-2038)
- 社内資料:ダルナビルの薬物動態に及ぼすリトナビルの影響(TMC114-C114)
- 社内資料:ダルナビルの排泄の検討(TMC114-C109)
- 社内資料:コビシスタットの排泄の検討(GS-US-216-0111)
- 社内資料:ダルナビル/リトナビルの小児HIV-1感染患者に対する臨床試験(TMC114-C230)(2019年6月18日承認、CTD2.7.3-3.2.1)
- Sekar V, et al.:Clin Pharmacokinet. 2010;49(5):343-350
- 社内資料:ダルナビル・コビシスタット配合剤の妊婦における薬物動態の検討(TMC114HIV3015)
- 社内資料:ダルナビルのin vitro酵素阻害に関する検討(TMC114-NC123)
- 社内資料:ダルナビルのトランスポーターに関する検討(TMC114-NC137)
- 社内資料:コビシスタットのin vitro酵素阻害に関する検討(AD-216-2028)
- 社内資料:コビシスタットのin vitro酵素阻害に関する検討(AD-216-2029)
- 社内資料:コビシスタットのトランスポーターに関する検討(AD-216-2099)
- 社内資料:コビシスタットのトランスポーターに関する検討(AD-216-2100)
- 社内資料:コビシスタットのトランスポーターに関する検討(AD-216-2094)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤のHIV-1感染患者に対する臨床成績(TMC114FD2HTX3001)(2019年6月18日承認、CTD2.7.3-3.1.1)
- 社内資料:ダルナビル・コビシスタット・エムトリシタビン・テノホビル アラフェナミド配合剤のHIV-1感染患者に対する臨床成績(TMC114IFD3013)(2019年6月18日承認、CTD2.7.3-3.1.3)
- Koh Y, et al.:J Biol Chem. 2007;282(39):28709-28720
- 社内資料:ダルナビルの作用機序(TMC114-0009-VRR)
- King NM, et al.:J Virol. 2004;78(21):12012-12021
- 社内資料:ダルナビルの作用機序(TMC114-0003-VRR)
- 社内資料:ダルナビルの作用機序(TMC114-0004-VRR)
- 社内資料:ダルナビルの抗ウイルス作用(TMC114-0014-VRR)
- 社内資料:ダルナビルの抗ウイルス作用(TMC114-0002-VRR)
- 社内資料:ダルナビルの抗ウイルス作用(TMC114-0011-VRR)
- 社内資料:ダルナビルの抗ウイルス作用(TMC114-0016-VRR)
- 社内資料:ダルナビルの抗ウイルス作用(TMC114-0006-VRR)
- 社内資料:ダルナビルの薬剤耐性(TMC114-0012-VRR)
- 社内資料:ダルナビルの薬剤耐性(TMC114-0013-VRR)
- 社内資料:ダルナビルの薬剤耐性(TMC114-0005-VRR)
24. 文献請求先及び問い合わせ先
ヤンセンファーマ株式会社 メディカルインフォメーションセンター
〒101-0065 東京都千代田区西神田3-5-2
フリーダイヤル 0120-183-275
https://www.janssenpro.jp
26. 製造販売業者等
26.1 製造販売元(輸入)
ヤンセンファーマ株式会社
〒101-0065 東京都千代田区西神田3-5-2