エプジコム配合錠の添付文書
- 商品名:
- エプジコム配合錠
- 一般名:
- アバカビル+ラミブジン(ABC/3TC)
- 略称 :
- EZC

添付文書の読み方
ここで提供している添付文書情報は、2025年1月現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
抗ウイルス化学療法剤
アバカビル+ラミブジン(ABC/3TC)

- ** 2024年8月改訂(第7版)
- * 2023年8月改訂(第6版)
規制区分:劇薬、処方箋医薬品注)
注)注意-医師等の処方箋により使用すること
| 日本標準商品分類番号 | 87625 |
|---|
| 貯法 | 室温保存 |
|---|---|
| 有効期間 | 3年 |
| 承認番号 | 22100AMX00411 |
|---|---|
| 販売開始 | 2005年1月 |
1. 警告
1.1 過敏症
1.1.1
海外の臨床試験において、アバカビル投与患者の約5%に過敏症の発現を認めており、まれに致死的となることが示されている。アバカビルによる過敏症は、通常、アバカビル含有製剤による治療開始6週以内(中央値11日)に発現するが、その後も継続して観察を十分に行うこと。[1.1.2-1.1.5、2.1、8.2、8.3、11.1.1、15.1.1参照]
1.1.2
アバカビルによる過敏症では以下の症状が多臓器及び全身に発現する。
- 皮疹
- 発熱
- 胃腸症状(嘔気、嘔吐、下痢、腹痛等)
- 疲労感、倦怠感
- 呼吸器症状(呼吸困難、咽頭痛、咳等) 等
このような症状が発現した場合は、直ちに担当医に報告させ、アバカビルによる過敏症が疑われたときは本剤の投与を直ちに中止すること。[1.1.1、1.1.3-1.1.5、2.1、8.2、8.3、11.1.1、15.1.1参照]
1.1.3
アバカビルによる過敏症が発現した場合には、決してアバカビル含有製剤を再投与しないこと。本製剤の再投与により数時間以内にさらに重篤な症状が発現し、重篤な血圧低下が発現する可能性及び死に至る可能性がある。[1.1.1、1.1.2、1.1.4、1.1.5、2.1、8.2、8.3、11.1.1、15.1.1参照]
1.1.4
呼吸器疾患(肺炎、気管支炎、咽頭炎)、インフルエンザ様症候群、胃腸炎、又は併用薬による副作用と考えられる症状が発現した場合あるいは胸部X線像異常(主に浸潤影を呈し、限局する場合もある)が認められた場合でも、アバカビルによる過敏症の可能性を考慮し、過敏症が否定できない場合は本剤の投与を直ちに中止し、決して再投与しないこと。[1.1.1-1.1.3、1.1.5、2.1、8.2、8.3、11.1.1、15.1.1参照]
1.1.5
患者に過敏症について必ず説明し、過敏症を注意するカードを常に携帯するよう指示すること。また、過敏症を発現した患者には、アバカビル含有製剤を二度と服用しないよう十分指導すること。[1.1.1-1.1.4、2.1、8.2、8.3、11.1.1、15.1.1参照]
1.2
B型慢性肝炎を合併している患者では、ラミブジンの投与中止により、B型慢性肝炎が再燃するおそれがあるので、本剤の投与を中断する場合には十分注意すること。特に非代償性の場合、重症化するおそれがあるので注意すること。[9.1.2参照]
2. 禁忌(次の患者には投与しないこと)
2.1
本剤の成分に対し過敏症の既往歴のある患者[1.1.1-1.1.5、8.2、8.3、11.1.1、15.1.1参照]
2.2
重度の肝障害患者[9.3.1、16.6.2参照]
3. 組成・性状
3.1 組成
| 販売名 | エプジコム配合錠 |
|---|---|
| 有効成分 | 1錠中 ラミブジン300mg アバカビル硫酸塩702mg(アバカビルとして600mg) |
| 添加剤 | 結晶セルロース、デンプングリコール酸ナトリウム、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール400、ポリソルベート80、黄色5号 |
3.2 製剤の性状
| 販売名 | エプジコム配合錠 |
|---|---|
| 剤形・性状 | だいだい色のフィルムコーティング錠 |
| 識別コード | GS FC2 |
| 表 (長径×短径) |
 20.3mm×8.9mm |
| 裏 |  |
| 側面 (厚さ) |
 8.3mm |
| 質量 | 1414mg |
4. 効能又は効果
HIV感染症
5. 効能又は効果に関連する注意
5.1
無症候性ヒト免疫不全ウイルス(HIV)感染症に関する治療開始については、CD4リンパ球数及び血漿中HIV RNA量が指標とされている。よって、本剤の使用にあたっては、患者のCD4リンパ球数及び血漿中HIV RNA量を確認するとともに、最新のガイドライン1)~3)を確認すること。
*5.2
本剤はラミブジン及びアバカビルの固定用量を含有する配合剤であるので、ラミブジン又はアバカビルの用量調節が必要な次の患者には個別のラミブジン製剤(エピビル錠)又はアバカビル製剤(ザイアジェン錠)を用いること。
- 腎機能障害(クレアチニンクリアランス(Ccr)が30mL/min未満)を有する患者[9.2.1、9.2.2、16.6.1参照]
- 軽度又は中等度の肝障害患者[9.3.2、16.6.2参照]
- 12歳未満の小児患者[9.7参照]
- 体重40kg未満の患者
- アバカビル又はラミブジンのいずれかによる副作用が疑われ、本剤の投与を中止した患者
5.3
本剤のHIV-2感染症患者に対する有効性・安全性は確認されていない。
6. 用法及び用量
通常、成人には1回1錠(ラミブジンとして300mg及びアバカビルとして600mg)を1日1回経口投与する。
7. 用法及び用量に関連する注意
7.1
本剤と他の抗HIV薬との併用療法において、因果関係が特定されない重篤な副作用が発現し、治療の継続が困難であると判断された場合には、本剤若しくは併用している他の抗HIV薬の一部を減量又は休薬するのではなく、原則として本剤及び併用している他の抗HIV薬の投与をすべて一旦中止すること。
7.2
本剤はラミブジン及びアバカビルの固定用量を含有する配合剤であるので、本剤に加えてラミブジン含有製剤又はアバカビル含有製剤を併用投与しないこと。
7.3
HIVは感染初期から多種多様な変異株を生じ、薬剤耐性を発現しやすいことが知られているので、本剤は他の抗HIV薬と併用すること。[18.3.1、18.3.2参照]
7.4
ラミブジンの薬剤耐性プロファイル等のウイルス学的特性はエムトリシタビンと類似しているので、本剤とエムトリシタビンを含む製剤を併用しないこと。また、エムトリシタビンを含む抗HIV療法においてウイルス学的効果が得られず、HIV-1逆転写酵素遺伝子のM184V/I変異が認められた場合、エムトリシタビンを本剤に変更するのみで効果の改善は期待できない。[18.3.1参照]
8. 重要な基本的注意
8.1
本剤はHIV感染症治療の経験を有する医師が投与を行うこと。
8.2
本剤の再投与を考慮する際は、次のことに注意すること。[1.1.1-1.1.5、2.1、8.3、11.1.1、15.1.1参照]
- アバカビルによる過敏症に関連する症状は、再投与により初回より重篤な再発が認められる。重篤な血圧低下をきたし死に至る可能性があるので、アバカビルによる過敏症が疑われた患者には、決して再投与しないこと。
- アバカビル含有製剤を中止した理由を再度検討し、アバカビルと過敏症との関連性が否定できない場合は再投与しないこと。
- 投与中止前に過敏症の主な症状(皮疹、発熱、胃腸症状等)の1つのみが発現していた患者には、本剤の有益性が危険性を上回ると判断される場合にのみ、必要に応じて入院のもとで投与を行うこと。
- 過敏症の症状又は徴候が認められていなかった患者に対しても、直ちに医療施設に連絡できることを確認した上で投与を行うこと。
*8.3
本剤の使用に際しては、国内外のガイドライン等の最新の情報を参考に、患者又は患者に代わる適切な者に、次の事項についてよく説明し同意を得た後、使用すること。
- 本剤はHIV感染症の根治療法薬ではないことから、日和見感染症を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので、本剤投与開始後の身体状況の変化については、すべて担当医に報告すること。
- アバカビルの投与後過敏症が発現し、まれに致死的となることが報告されている。過敏症を注意するカードに記載されている徴候又は症状である発熱、皮疹、疲労感、倦怠感、胃腸症状(嘔気、嘔吐、下痢、腹痛等)及び呼吸器症状(呼吸困難、咽頭痛、咳等)等が発現した場合は、直ちに担当医に報告し、本剤の服用を中止すべきか否か指示を受けること。また、過敏症を注意するカードは常に携帯すること。[1.1.1-1.1.5、2.1、8.2、11.1.1、15.1.1参照]
- アバカビル含有製剤の再投与により重症又は致死的な過敏症が数時間以内に発現する可能性がある。したがって、本剤の服用を中断した後に再びアバカビル含有製剤を服用する際には、必ず担当医に相談すること。担当医又は医療施設を変わる場合には本剤の服用歴がある旨を新しい担当医に伝えること。[1.1.1-1.1.5、2.1、8.2、11.1.1、15.1.1参照]
- 本剤はラミブジン及びアバカビルの固定用量を含有する配合剤であるので、本剤に加えてラミブジン含有製剤又はアバカビル含有製剤をさらに追加して服用しないこと。
8.4
本剤を含む抗HIV薬の多剤併用療法を行った患者で、免疫再構築症候群が報告されている。投与開始後、免疫機能が回復し、症候性のみならず無症候性日和見感染(マイコバクテリウムアビウムコンプレックス、サイトメガロウイルス、ニューモシスチス等によるもの)等に対する炎症反応が発現することがある。また、免疫機能の回復に伴い自己免疫疾患(甲状腺機能亢進症、多発性筋炎、ギラン・バレー症候群、ブドウ膜炎等)が発現するとの報告があるので、これらの症状を評価し、必要時には適切な治療を考慮すること。
8.5
膵炎が発症する可能性があるので、血清アミラーゼ、血清リパーゼ、トリグリセリド等の生化学的検査を定期的に行うこと。[9.1.1、11.1.3参照]
8.6
重篤な血液障害、乳酸アシドーシス、脂肪沈着による重度の肝腫大(脂肪肝)、横紋筋融解症、ニューロパシー、錯乱、痙攣、心不全、皮膚粘膜眼症候群、中毒性表皮壊死融解症があらわれることがあるので、定期的に検査を行うなど観察を十分に行うこと。[9.2.2、11.1.2、11.1.4-11.1.8参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 膵炎を発症する可能性のある患者(膵炎の既往歴のある患者、膵炎を発症させることが知られている薬剤との併用療法を受けている患者)
膵炎を再発又は発症する可能性がある。本剤の適用を考える場合には、他に十分な効果の認められる治療法がない場合にのみ十分注意して行うこと。[8.5、11.1.3参照]
9.1.2 B型肝炎ウイルス感染を合併している患者
本剤の投与を中断する場合には十分注意すること。B型慢性肝炎を合併している患者では、本剤の投与中止により、B型慢性肝炎が再燃するおそれがある。特に非代償性の場合、重症化するおそれがある。[1.2参照]
9.2 腎機能障害患者
*9.2.1 腎機能障害(Ccrが30mL/min未満)を有する患者
ラミブジンの高い血中濃度が持続するおそれがある。[5.2、16.6.1参照]
*9.2.2 腎機能障害(Ccrが30~49mL/min)を有する患者
血液検査等をより頻回に行うなど、慎重に患者の状態を観察すること。ラミブジンに関連する副作用の発現が疑われる場合は、個別のラミブジン製剤又はアバカビル製剤を用いてラミブジンの用量調節を考慮すること。ラミブジンの高い血中濃度が持続するおそれがある。[5.2、8.6、16.6.1参照]
9.3 肝機能障害患者
9.3.1 重度の肝障害患者
投与しないこと。アバカビルの血中濃度が上昇することにより、副作用が発現するおそれがある。[2.2、16.6.2参照]
9.3.2 軽度又は中等度の肝障害患者
アバカビルの血中濃度が上昇することにより、副作用が発現するおそれがある。[5.2、16.6.2参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
動物実験においてラミブジン及びアバカビルに関して次のことが報告されている。
9.5.1 ラミブジン
ラミブジンはヒト胎盤を通過する。出生児の血清中ラミブジン濃度は、分娩時の母親の血清中及び臍帯血中濃度と同じであることが報告されている(外国人データ)。
動物実験(ウサギ)で胎児毒性(早期の胚死亡数の増加)が報告されている。
9.5.2 アバカビル
動物において、アバカビル又はその代謝物は胎盤を通過することが示されている。また、動物(ラットのみ)において、アバカビルの500mg/kg/日又はそれ以上の投与量(ヒト全身曝露量(AUC)の32~35倍)で、胚又は胎児に対する毒性(胎児の浮腫、変異及び奇形、吸収胚、体重減少、死産の増加)が認められたとの報告がある。
9.5.3 ラミブジン/アバカビル共通
ヌクレオシド系逆転写酵素阻害剤(NRTI)を子宮内曝露又は周産期曝露された新生児及び乳児において、ミトコンドリア障害によると考えられる軽微で一過性の血清乳酸値の上昇が報告されている。
非常にまれに発育遅延、てんかん様発作、他の神経疾患も報告されている。しかしながら、これら事象とNRTIの子宮内曝露、周産期曝露との関連性は確立していない。
9.6 授乳婦
授乳を避けさせること。一般に、HIVの乳児への移行を避けるため、あらゆる状況下においてHIVに感染した女性は授乳すべきでない。
9.6.1 ラミブジン
経口投与されたラミブジンはヒト乳汁中に排泄されることが報告されている(乳汁中濃度:<0.5-8.2μg/mL)4)(外国人データ)。
ラミブジンの母体血漿中濃度に対する乳汁中濃度の比は0.6~3.3であることが報告されている(外国人データ)。
乳児の血清中ラミブジン濃度は18~28ng/mLであったとの報告がある(外国人データ)。
9.6.2 アバカビル
アバカビルの母体血漿中濃度に対する乳汁中濃度の比は0.9であることが報告されている5)(外国人データ)。
9.7 小児等
ラミブジン又はアバカビルの用量調節が必要である12歳未満の小児患者には、個別のラミブジン製剤(エピビル錠)又はアバカビル製剤(ザイアジェン錠)を用いること。[5.2参照]
9.8 高齢者
患者の肝、腎、及び心機能の低下、合併症、併用薬等を十分考慮し慎重に投与すること。
10. 相互作用
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| スルファメトキサゾール・トリメトプリム | ラミブジンのAUCが43%増加し、全身クリアランスが30%、腎クリアランスが35%減少したとの報告がある。 | 腎臓における排泄がラミブジンとトリメトプリムで競合すると考えられている。 |
| ソルビトール | 経口ソルビトール溶液(ソルビトールとして3.2g、10.2g、13.4g)とラミブジンの併用により、ラミブジンのAUCが減少した(それぞれ18%、36%、42%減少)との報告がある。 | ソルビトールによりラミブジンの吸収が抑制されると考えられている。 |
| アルコール(飲酒) [16.4.2、16.7.1、16.7.2参照] |
アバカビルの代謝はエタノールによる影響を受ける。アバカビルのAUCが約41%増加したが、エタノールの代謝は影響を受けなかったとの報告がある16)。 | アルコールデヒドロゲナーゼの代謝基質として競合すると考えられている。 |
| メサドン塩酸塩 | メサドンのクリアランスが22%増加したことから、併用する際にはメサドン塩酸塩の増量が必要となる場合があると考えられる。なお、アバカビルの血中動態は臨床的意義のある影響を受けなかった(Cmaxが35%減少し、tmaxが1時間延長したが、AUCは変化しなかった)。 | 機序不明 |
| リオシグアト[16.7.2参照] | 本剤とリオシグアトの併用により、リオシグアトのAUCが増加するおそれがある。本剤との併用が必要な場合は、患者の状態に注意し、必要に応じてリオシグアトの減量を考慮すること。 | アバカビルのCYP1A1阻害作用によりリオシグアトの代謝が阻害される。 |
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 過敏症(頻度不明)
アバカビルの投与により発熱又は皮疹を伴う多臓器及び全身性の過敏症があらわれることがあるので、観察を十分に行い、以下に示すような徴候又は症状があらわれた場合には、直ちに投与を中止し、適切な処置を行うこと。[1.1.1-1.1.5、2.1、8.2、8.3、15.1.1参照]
- 皮膚
皮疹注1)(通常、斑状丘疹性皮疹又はじん麻疹)、多形紅斑 - 消化器
嘔気注1)、嘔吐注1)、下痢注1)、腹痛注1)、口腔潰瘍 - 呼吸器
呼吸困難注1)、咳注1)、咽頭痛、急性呼吸促迫症候群、呼吸不全 - 精神神経系
頭痛注1)、感覚異常 - 血液
リンパ球減少 - 肝臓
肝機能検査値異常注1)(AST、ALT等の上昇)、肝不全 - 筋骨格
筋痛注1)、筋変性(横紋筋融解、筋萎縮等)、関節痛、CK上昇 - 泌尿器
クレアチニン上昇、腎不全 - 眼
結膜炎 - その他
発熱注1)、嗜眠注1)、倦怠感注1)、疲労感注1)、浮腫、リンパ節腫脹、血圧低下、粘膜障害、アナフィラキシー
注1)アバカビルによる過敏症発現患者のうち10%以上にみられた症状
11.1.2 重篤な血液障害(頻度不明)
赤芽球癆、汎血球減少、貧血、白血球減少、好中球減少、血小板減少[8.6参照]
11.1.3 膵炎(頻度不明)
血清アミラーゼ、血清リパーゼ、トリグリセリド等の検査値の上昇がみられた場合には、直ちに本剤の投与を中止すること。また、重度の腹痛、悪心・嘔吐等の症状がみられた場合にも直ちに本剤の投与を中止し、生化学的検査(血清アミラーゼ、血清リパーゼ、トリグリセリド等)及び画像診断等による観察を十分行うこと。[8.5、9.1.1参照]
11.1.4 乳酸アシドーシス、脂肪沈着による重度の肝腫大(脂肪肝)(頻度不明)
乳酸アシドーシス又は肝毒性が疑われる臨床症状や検査値異常が認められた場合には、本剤の投与を一時中止すること。特に、肝疾患の危険因子を有する患者においては注意すること。ラミブジン及びアバカビルを含むNRTIの単独投与又はこれらの併用療法により、重篤な乳酸アシドーシス(全身倦怠、食欲不振、急な体重減少、胃腸障害、呼吸困難、頻呼吸等)、肝毒性(脂肪沈着による重度の肝腫大、脂肪肝を含む)が、女性に多く報告されている。[8.6参照]
11.1.5 横紋筋融解症(頻度不明)
[8.6参照]
11.1.6 ニューロパシー、錯乱、痙攣(頻度不明)
[8.6参照]
11.1.7 心不全(頻度不明)
[8.6参照]
11.1.8 皮膚粘膜眼症候群(Stevens-Johnson症候群)、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)
[8.6参照]
11.2 その他の副作用
| 1%~17%未満 | 1%未満 | 頻度不明 | |
|---|---|---|---|
| 血液 | リンパ節症、平均赤血球容積(MCV)増加、リンパ球減少 | ||
| 消化器 | 嘔気 | 下痢、腹痛、嘔吐、胃炎、食欲不振 | 痔核、腹部痙直、消化不良、鼓腸放屁 |
| 全身症状 | 倦怠感、発熱、頭痛、体脂肪の再分布/蓄積(胸部、体幹部の脂肪増加、末梢部、顔面の脂肪減少、野牛肩、血清脂質増加、血糖増加)、無力症 | 体温調節障害、疼痛、体重減少、疲労、疲労感 | |
| 肝臓 | 肝機能検査値異常(AST、ALT等の上昇) | ||
| 腎臓 | 血清クレアチニン上昇 | ||
| 筋骨格 | 筋肉痛 | 関節痛、筋痙直、骨痛 | |
| 精神神経系 | めまい、睡眠障害、うつ病 | 感情障害、不安感、末梢神経障害、嗜眠、錯感覚 | |
| 代謝・内分泌系 | 血中尿酸上昇 | 脱水(症)、高乳酸塩血症、アミラーゼ上昇 | |
| 循環器 | 心筋症 | ||
| 呼吸器 | 咳、呼吸困難 | 肺炎、咽頭痛、気管支炎、鼻炎、副鼻腔炎、耳管炎、呼吸障害、上気道炎 | |
| 過敏症 | アレルギー反応 | ||
| 皮膚 | 発疹(皮膚炎、湿疹、皮疹を含む) | そう痒 | 脱毛、発汗、痤瘡・毛嚢炎 |
| その他 | トリグリセリド上昇・血清コレステロール上昇 | CK上昇、血糖値上昇 | 重炭酸塩上昇、重炭酸塩低下、血糖値低下、総蛋白上昇、総蛋白低下、敗血症 |
注)発現頻度には使用成績調査の結果を含む
13. 過量投与
13.1 処置
ラミブジンは血液透析により一部除去される(ラミブジン300mg投与時に、投与約2時間後から4時間血液透析したとき、AUC0-infが約24%低下することが報告されている)34)。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1
海外で実施されたプロスペクティブ試験(1956例)において、アバカビルの投与開始前にHLA-B*5701のスクリーニングを実施しない群と、スクリーニングを実施しHLA-B*5701保有者を除外した群における臨床症状から疑われる過敏症の発現頻度が、それぞれ7.8%(66/847)、3.4%(27/803)、皮膚パッチテストにより確認された過敏症の発現頻度が、それぞれ2.7%(23/842)、0.0%(0/802)であり、HLA-B*5701のスクリーニングの実施により過敏症の発現頻度が統計学的に有意に低下する(p<0.0001)ことが示された。また、本試験結果ではHLA-B*5701をスクリーニングしない群において臨床症状から過敏症が疑われた66例中30例、皮膚パッチテストにて確認された過敏症症例23例全例がHLA-B*5701を有していた。
日本人における過敏症とHLA-B*5701保有の関連性については不明であり、HLA-B*5701の保有率は白人では5~8%、日本人では0.1%との報告がある。[1.1.1-1.1.5、2.1、8.2、8.3、11.1.1参照]
15.1.2
抗HIV薬の多剤併用療法を受けている患者を対象に心筋梗塞の発現頻度を調査したプロスペクティブ観察疫学研究において、アバカビルの使用開始から6ヵ月以内の患者で心筋梗塞のリスクが増加するとの報告があるが、臨床試験の統合解析を実施した結果、対照群と比較してアバカビル投与群の過度な心筋梗塞のリスクは認められなかった。アバカビルと心筋梗塞の関連については、現在のところ結論は出ていない。予防措置として、アバカビルを含む抗HIV療法を開始する場合には、冠動脈性心疾患の潜在的リスクを考慮し、高血圧、高脂血症、糖尿病、喫煙等の改善可能なすべてのリスク因子を最小化させるための措置をとること。
15.2 非臨床試験に基づく情報
15.2.1 ラミブジン
遺伝毒性試験において弱い染色体異常誘発作用を示したとの報告がある。また、長期のがん原性試験において発がん性を認めなかったとの報告がある。
ヒト末梢血リンパ球を用いた染色体異常試験では300μg/mL以上、マウスリンパ腫細胞を用いた遺伝子突然変異試験では2000μg/mL以上で陽性を示した。
マウス及びラットを用いた長期のがん原性試験では、臨床用量におけるヒト全身曝露量(AUC)の10倍(マウス)及び58倍(ラット)までの曝露量において、発がん性は認められなかった。
15.2.2 アバカビル
(1)
細菌を用いた試験では変異原性を認めなかったが、ヒトリンパ球を用いたin vitro染色体異常試験、マウスリンフォーマ試験及びin vivo小核試験では陽性を認めた。これらの結果は、in vivo及びin vitroにおいて、本剤の高濃度を用いた場合に弱い染色体異常誘発作用を有することを示している。
(2)
マウス及びラットにおける長期がん原性試験において、包皮腺、陰核腺、肝臓、膀胱、リンパ節、皮下組織等に悪性腫瘍がみられたとの報告がある(ヒト全身曝露量(AUC)の24~32倍。ただし包皮腺(ヒトにおいて該当する器官は存在しない)の腫瘍については6倍。)ので、ヒトに対する潜在的危険性と治療上の有益性を十分に検討すること。
(3)
アバカビルを2年間投与したマウス及びラットにおいて、軽度心筋変性が認められた(ヒト全身曝露量(AUC)の7~24倍の用量)。
16. 薬物動態
16.1 血中濃度
16.1.1 単回経口投与
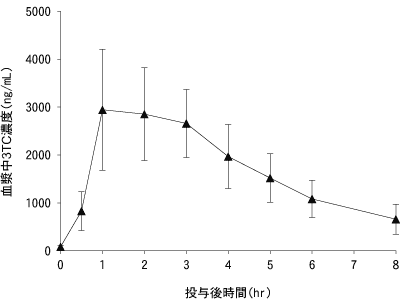
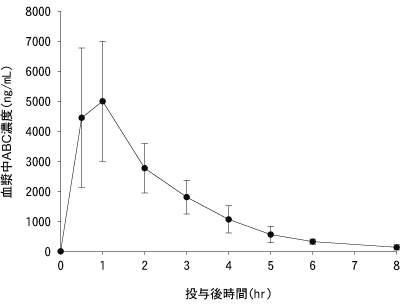
HIV感染症患者9例に本剤を空腹時単回投与した時のラミブジン、アバカビルの血漿中濃度の推移を図-1及び図-2に、薬物動態パラメータを表-1に示した6)。
| Cmax (μg/mL) |
AUClast (h・μg/mL) |
AUC0-τ (h・μg/mL) |
tmax注1) (h) |
t1/2 (h) |
|
|---|---|---|---|---|---|
| ラミブジン | 3.58±0.61 | 13.81±3.56 | 16.30±5.058 | 2.00 (1.00-3.00) |
2.49±0.55 |
| アバカビル | 5.68±2.04 | 12.56±4.01 | 12.89±4.22 | 1.00 (0.50-1.03) |
1.50±0.16 |
平均値±標準偏差、9例
注1)中央値(範囲)
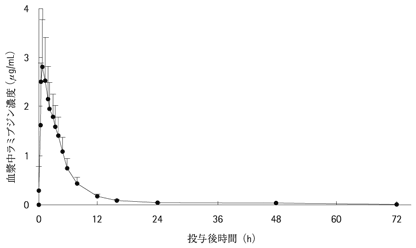
健康成人76例にドルテグラビル・ラミブジン50mg・300mgを空腹時に単回経口投与した時のラミブジンの血漿中濃度の推移を図-3に、薬物動態パラメータを表-2に示した37)(外国人データ)。
| AUC0-inf (μg・h/mL) |
Cmax (μg/mL) |
Tmax (h)注1) |
t1/2 (h) |
|---|---|---|---|
| 13.59 (17.99) |
3.22 (29.30) |
1.00 (0.50,3.50) |
18.63 (26.85) |
16.1.2 生物学的同等性
健康成人25例に、本剤1錠、及びエピビル錠(ラミブジン150mgを含有する製剤)及びザイアジェン錠(アバカビル300mgを含有する製剤)各2錠を空腹時単回経口投与し、生物学的同等性を評価した。本剤投与時とラミブジン製剤及びアバカビル硫酸塩製剤の併用投与時のラミブジン及びアバカビルのAUClast、AUC∞及びCmaxは、生物学的同等性の判定基準(平均値の比の90%信頼区間が0.80~1.25の範囲内)を満たし、生物学的同等性が示された(外国人データ)。
16.2 吸収
16.2.1 食事の影響
健康成人25例に、高脂肪食(約1000kcal、約50%が脂肪由来)摂取後に本剤を経口投与した時、空腹時投与時と比較して、ラミブジンのAUClast、AUC∞、Cmax、及びアバカビルのAUClast、AUC∞に変化は認められなかったが、アバカビルのCmaxは24%低下した(外国人データ)。
16.3 分布
16.3.1 ラミブジン
(1)脳脊髄液への移行
成人HIV感染症患者にラミブジン4~10mg/kg注)を1日2回2週間以上反復経口投与した時、投与2時間後の脳脊髄液中濃度は血中濃度の約6%であった7)(外国人データ)。
16.3.2 アバカビル
(1)分布容積
HIV感染症患者6例を対象にアバカビル150mgを静脈内投与注)した時の見かけの分布容積は約0.86L/kgであり、広く組織に分布することが示唆された8),9)(外国人データ)。
(2)脳脊髄液への移行
HIV感染症患者におけるアバカビルの脳脊髄液(CSF)への移行は良好で、血漿中AUCに対するCSF中AUCの比は31~44%であった10)(外国人データ)。アバカビル600mg1日2回投与時の最高濃度の実測値はIC50(0.08μg/mLあるいは0.26μM)の9倍超であった9)(外国人データ)。
(3)血漿蛋白結合率
In vitroにおいて、アバカビルは10μg/mLまでの添加濃度範囲で、ヒト血漿蛋白結合率は49%と一定であった9)。
(4)血球移行性
血液及び血漿中放射能濃度が同じであったことから、アバカビルは血球に直ちに分布することが示された9)。
16.4 代謝
16.4.1 ラミブジン
ヒトでの主代謝物はトランス-スルホキシド体(1-[(2R,5S)-trans-2-hydroxymethyl-1,3-oxathiolan-3-oxide-5-yl]cytosine)であった11)(外国人データ)。
16.4.2 アバカビル
ヒトでの主代謝物は、5'-カルボン酸体及び5'-グルクロン酸抱合体であった10)(外国人データ)。ヒト肝由来試料を用いたin vitro試験から、アバカビルは肝可溶性画分により酸化的代謝を受け5'-カルボン酸体を生成したが、肝ミクロソーム画分ではアバカビルの酸化的代謝は起こらなかった。アバカビルの酸化的代謝にはCYPではなく、アルコールデヒドロゲナーゼ/アルデヒドデヒドロゲナーゼが関与していた。なお、これらの代謝物には抗ウイルス活性はなかった。[10.2、16.7.1、16.7.2参照]
アバカビルは細胞内で活性代謝物であるカルボビル三リン酸に代謝される。HIV感染症患者20例にアバカビル300mg1日2回投与した時の定常状態における細胞内カルボビル三リン酸の半減期は20.6時間であった(外国人データ)。
16.5 排泄
16.5.1 ラミブジン
成人HIV感染症患者にラミブジン2mg/kg注)を経口投与した時、投与後12時間尿中にトランス-スルホキシド体が投与量の5.2%排泄された。また、血中濃度が定常状態での未変化体の尿中排泄率は投与量の約70%であり、腎排泄がラミブジンの体内からの除去の主要な経路であることが示された11)(外国人データ)。
16.5.2 アバカビル
HIV感染症患者6例を対象に14C標識アバカビル600mgを単回経口投与後、薬物体内動態を検討した。総放射能の約99%が排泄され、主な排泄経路は尿(約83%)であり、糞中には約16%排泄された。尿中に排泄された放射能の約1%は未変化体であり、約30%が5'-カルボン酸体、約36%が5'-グルクロン酸抱合体であった10)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
(1)ラミブジン
腎機能の低下したHIV感染症患者にラミブジン300mgを単回経口投与した時、Ccrの低下につれてAUC及び最高血中濃度が増加し、半減期が延長し、見かけの全身クリアランスが減少した12)(外国人データ)。[5.2、9.2.1、9.2.2参照]
(2)アバカビル
腎機能障害患者(GFR:<10mL/min)におけるアバカビルの薬物動態は、腎機能が正常な患者の薬物動態と同様であった13)(外国人データ)。[5.2、9.2.1、9.2.2参照]
16.6.2 肝障害患者
(1)ラミブジン
中等度及び重度の肝障害を有する患者における成績より、ラミブジンの薬物動態は、肝障害によって重大な影響を受けないことが示されている14)(外国人データ)。[2.2、5.2、9.3.1参照]
(2)アバカビル
軽度の肝障害(Child-Pugh分類の合計点数:5)を有するHIV感染症患者におけるアバカビルの薬物動態を検討した結果、AUC及び消失半減期は肝障害を有さないHIV感染症患者のそれぞれ1.89倍及び1.58倍であった。代謝物の体内消失速度にも変化が認められたが、AUCは肝障害による影響を受けなかった15)(外国人データ)。なお、これら患者に対する推奨投与量は明らかでない。[2.2、5.2、9.3.1、9.3.2参照]
16.7 薬物相互作用
16.7.1 In vitro試験
アバカビルは、アバカビルの主代謝酵素であるアルコールデヒドロゲナーゼ/アルデヒドデヒドロゲナーゼを阻害しなかった。[10.2、16.4.2、16.7.2参照]
また、in vitro試験において、アバカビルはCYP1A1を阻害し、CYP3A4もわずかに阻害した35)が、CYP2D6及び2C9を阻害しなかった36)。
ヒト肝スライスを用いたin vitro試験において、HIVプロテアーゼ阻害剤であるアンプレナビルはアバカビルの代謝を阻害しなかった。
16.7.2 臨床薬物相互作用試験
HIV感染症患者25例を対象にアバカビル600mgをエタノール0.7g/kgと併用して単回投与した場合、アバカビルのAUC∞の上昇及びt1/2の延長がみられたが臨床上重要なものではなかった。また、アバカビルはエタノールの薬物動態に影響を示さなかった16)(外国人データ)。[10.2、16.4.2、16.7.1参照]
HIV感染症患者15例を対象にアバカビル600mgとジドブジン300mg及びラミブジン150mg注)のどちらか1剤あるいは両剤を併用した場合、いずれの併用においても併用薬によるアバカビル血中濃度への影響はみられなかった。一方、アバカビルと併用したラミブジンのAUC∞及びCmaxは、ジドブジン併用、非併用に関わらずいずれも低下した。また、アバカビルと併用したジドブジンは、ラミブジン併用時及び非併用時においてAUC∞の上昇がみられたが、Cmaxは低下した。これらの変化は臨床上重要なものではなかった17)(外国人データ)。
アバカビル・ドルテグラビル・ラミブジン600mg・50mg・300mg注)を投与中の成人HIV感染症患者にリオシグアト0.5mgを単回経口投与した時、リオシグアトのAUCが健康成人に単独投与したヒストリカルコントロールと比べて約2.6倍に増加した35),38)(外国人データ)。[10.2参照]
注)本剤の承認された用法及び用量は、「通常、成人には1回1錠(ラミブジンとして300mg及びアバカビルとして600mg)を1日1回経口投与する。」である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 海外第III相試験(CNA30021)
治療経験がない成人のHIV感染症患者770例を対象としてアバカビルの投与回数を比較する無作為二重盲検比較試験(ラミブジン300mg1日1回とエファビレンツ600mg1日1回の併用による、アバカビル600mg1日1回投与群384例又はアバカビル300mg1日2回投与群386例)を実施した。投与48週後にHIV-1 RNA量が400copies/mL未満であった患者の比率は、アバカビル600mg1日1回投与群、300mg1日2回投与群ともに72%であった。さらに、投与48週後にHIV-1 RNA量が50copies/mL未満であった患者の比率は、アバカビル600mg1日1回投与群が66%、アバカビル300mg1日2回投与群が68%であった(図-1)。
また、投与48週後のCD4リンパ球数の増加量(中央値)は、それぞれ188/mm3、200/mm3であった。
(Intent-to-treat analysis)
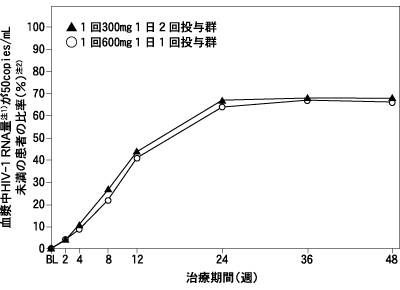
注1)Roche AMPLICOR HIV-1 MONITOR
注2)治療が中止されることなく血漿中HIV-1 RNA量が50copies/mL未満を達成しかつ維持された患者の比率
なお、本試験における試験成績の要約を表-1に示した。
| 結果 | アバカビル600mg + ラミブジン+ (n=384) |
アバカビル300mg + ラミブジン+ (n=386) |
|---|---|---|
| レスポンダー注1) | 66%(72%) | 68%(72%) |
| ウイルス学的な治療失敗注2) | 10%(4%) | 8%(4%) |
| 有害事象による中止 | 13% | 11% |
| その他の理由による中止注3) | 11% | 13% |
(n=Intent-to-treat analysis)
注1)血漿中HIV-1 RNA量が50copies/mL未満(400copies/mL未満)となり投与48週後まで維持された患者の比率
注2)血漿中HIV-1 RNA量が50copies/mL未満(400copies/mL未満)となったが投与48週後までにリバウンドを起こした患者、ウイルス学的に治療が失敗した患者、ウイルス学的な効果が不十分と判断された患者
注3)同意の撤回、試験途中でフォローアップ不可、プロトコール違反、症状の進行等
ラミブジン300mg及びアバカビル600mg1日1回併用投与群において、384例中283例(73.7%)に副作用が認められ、主な副作用はめまい73例(19.0%)、異常な夢62例(16.1%)、不眠54例(14.1%)、嘔気53例(13.8%)であった。
17.1.2 海外第III相試験(CAL30001)
抗HIV薬の治療経験がある18歳以上の患者182例を対象として本剤とアバカビル及びラミブジンの併用療法を比較する無作為オープン比較試験(テノホビル300mg1日1回と使用経験のないHIVプロテアーゼ阻害剤又は非核酸系逆転写酵素阻害剤1剤の併用による、本剤1日1回投与群94例又はアバカビル300mg1日2回+ラミブジン300mg1日1回投与群88例)を実施した。48週間の治療により、血漿中HIV-1 RNA AAUCMB値は、本剤投与群で-1.65log10 copies/mL、アバカビル+ラミブジン併用投与群で-1.83log10 copies/mLであり、非劣性であった。48週間の治療後の血漿中HIV-1 RNA量が50copies/mL未満の患者の比率はそれぞれ50%、47%と同等であり、また、血漿中HIV-1 RNA量が400copies/mL未満の患者の比率もそれぞれ54%、57%と同等であった。48週間の治療後のCD4リンパ球数の増加量(中央値)は、本剤投与群で47.5/mm3、アバカビル+ラミブジン併用投与群で95.0/mm3であった。
本剤1日1回投与群において、93例中45例(48.4%)に副作用が認められ、主な副作用は嘔気11例(11.8%)、下痢10例(10.8%)であった。
18. 薬効薬理
18.1 作用機序
18.1.1 ラミブジン
ラミブジンは細胞内でリン酸化され、HIVを感染させた細胞内での半減期が約12時間の活性化型の三リン酸化体に変換される18)。ラミブジン三リン酸化体はHIVの逆転写酵素によりデオキシシチジン三リン酸の代わりにウイルスDNA鎖に取り込まれ、DNA鎖の伸長を停止させることによりHIVの複製を阻害する19)。また、ラミブジン三リン酸化体はHIVの逆転写酵素を競合的に阻害する19)。一方、in vitroで、ヒト末梢血リンパ球、リンパ球系・単球-マクロファージ系の株化細胞20)及び種々のヒト骨髄前駆細胞に対するラミブジンの細胞毒性は弱かった。
18.1.2 アバカビル
アバカビルは細胞内で活性化型のカルボビル三リン酸に変換される。カルボビル三リン酸は天然基質デオキシグアノシン三リン酸に代わってウイルスDNA鎖に取り込まれ、DNA鎖の伸長を停止させることによりHIVの複製を阻害する。また、カルボビル三リン酸はHIV逆転写酵素を競合的に阻害する。21)~23)
18.2 抗ウイルス作用
18.2.1 ラミブジン
In vitroでのラミブジンのHIV-1(RF、GB8、U455及びIIIB)に対するIC50値は670nM以下、HIV-2 RODに対するIC50値は40nMであった20)。
In vitroでアバカビル、ジダノシン、ネビラピン、ザルシタビン及びジドブジンとの相加又は相乗作用が認められた24)。また、ラミブジンは単独で、ジドブジン耐性臨床分離株の平均p24抗原量を薬物無処置群に比べ66~80%低下させた(in vitro)。
In vitroでの26種のHIV-1臨床分離株[グループM(サブタイプA、B、C、D、E、F、G)]並びに3種類のHIV-2臨床分離株に対するラミブジンのIC50値(平均値)はHIV-1株及びHIV-2株でそれぞれ40nM(範囲は1~120nM)及び42nM(範囲は2~120nM)であった。
18.2.2 アバカビル
アバカビルのHIV-1に対するIC50値はHIV-1 IIIBに対して3.7~5.8μM、臨床分離株に対して0.26±0.18μM(n=8)、HIV-1 BaLに対して0.07~1.0μMであった。また、HIV-2に対するIC50値はHIV-2(Zy)に対して4.1μM、HIV-2 LAV-2に対して7.5μMであった。In vitroでNRTIのジダノシン、エムトリシタビン、ラミブジン、サニルブジン、テノホビル、ザルシタビン及びジドブジン、非ヌクレオシド系逆転写酵素阻害剤(NNRTI)のネビラピン、及びプロテアーゼ阻害剤のアンプレナビルとの相加又は相乗作用が認められた23)。また、ヒト末梢血単核球から活性化リンパ球を除いた場合に、より強い抗HIV作用を示したことから、アバカビルは静止細胞でより強く抗ウイルス作用を示すものと考えられる25)。
18.3 薬剤耐性
18.3.1 ラミブジン
ラミブジンを含む抗HIV薬で治療を受けたHIV-1感染症患者で発現するラミブジン耐性HIV-1には、HIV逆転写酵素の活性部位に近い184番目のアミノ酸のメチオニンからバリンへの変異(M184V)がみられる26)。このM184V変異の結果、ウイルスのラミブジンに対する感受性は著明に低下し26),27)、in vitroでのウイルスの複製能力は低下する28)。
In vitroにおいて、ジドブジン耐性臨床分離株にラミブジン耐性変異を導入すると、ジドブジンに対する感受性は回復することが確認されている。また、抗HIV薬の治療経験のない患者にジドブジン及びラミブジンを併用することにより、ジドブジン耐性ウイルスの出現が遅延する29)。さらに、抗HIV薬(ラミブジンを含む)の多剤併用療法はM184V変異ウイルスを有する患者と同様、抗HIV薬の治療経験のない患者においても有効性が確認されている30),31)。[7.3、7.4参照]
18.3.2 アバカビル
アバカビルに対して低感受性のHIV-1分離株がin vitro及びアバカビル投与患者から分離されており、いずれも逆転写酵素にM184V、K65R、L74V及びY115Fの変異が確認された。これらの変異を2種以上含むことにより、アバカビル感受性は1/10に低下した。臨床分離株ではM184V及びL74Vの変異が頻回に観察された21)。[7.3参照]
18.4 交差耐性
18.4.1 ラミブジン
ジドブジン及びサニルブジンは、ラミブジン耐性HIV-1に対し抗ウイルス活性を維持する27),29),32)。
アバカビルはM184V変異のみが認められているウイルスに対しては、抗ウイルス活性を維持する21)。
また、ジダノシン及びザルシタビンは、M184V変異ウイルスに対して感受性が低下するというin vitroでの報告があるが、これらの感受性の低下と臨床効果の関係は明らかにされていない33)。
18.4.2 アバカビル
2種以上のアバカビル関連耐性変異を獲得したHIV-1株のうち数種は、in vitroでラミブジン、ジダノシン及びザルシタビンに対して交差耐性を示し、一方、ジドブジン及びサニルブジンには感受性を示した21)。
アバカビルとHIVプロテアーゼ阻害剤とは標的酵素が異なることから、両者間で交差耐性を示す可能性は低く、NNRTIも逆転写酵素の結合部位が異なることから、交差耐性を示す可能性は低いものと考えられる。
19. 有効成分に関する理化学的知見
| 一般的名称 | ラミブジン(Lamivudine) |
|---|---|
| 化学名 | (-)-1-[(2R,5S)-2-hydroxymethyl-1,3-oxathiolan-5-yl]cytosine |
| 分子式 | C8H11N3O3S |
| 分子量 | 229.26 |
| 化学構造式 | 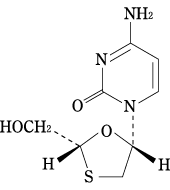 |
| 性状 | 白色~微黄白色の結晶性の粉末である。ジメチルスルホキシドに溶けやすく、水にやや溶けやすく、メタノール又はエタノール(99.5)にやや溶けにくく、ジエチルエーテルにほとんど溶けない。 |
| 融点 | 約176℃ |
| 分配係数 | -0.9(1-オクタノール/水系) |
| 一般的名称 | アバカビル硫酸塩(Abacavir Sulfate) |
|---|---|
| 化学名 | (-)-{(1S,4R)-4-[2-amino-6-(cyclopropylamino)purin-9-yl]cyclopenta-2-enyl}methanol hemisulfate |
| 分子式 | (C14H18N6O)2・H2SO4 |
| 分子量 | 670.74 |
| 化学構造式 | 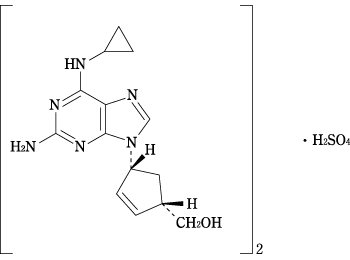 |
| 性状 | 白色~微黄白色の粉末である。トリフルオロ酢酸に溶けやすく、水にやや溶けやすく、メタノール及びエタノール(95)に溶けにくい。0.1mol/L塩酸試液及び希水酸化ナトリウム試液に溶ける。 |
| 融点 | 約219℃(分解) |
| 分配係数 |
1.20(pH7.1~7.3, 1-オクタノール/水) |
21. 承認条件
本剤を使用する場合は重篤な過敏症に留意し、過敏症の兆候又は症状が発現した場合には本剤の使用を中止する等の適切な処置をとるよう、医師に要請すること。
22. 包装
30錠[瓶、バラ]
23. 主要文献
- DHHS:Guidelines for Using Antiretroviral Agents Among HIV-Infected Adults and Adolescents. http://www.aidsinfo.nih.gov/Guidelines/
- 抗HIV治療ガイドライン. http://www.haart-support.jp/
- HIV感染症「治療の手引き」. http://www.hivjp.org/
- Moodley J, et al.:J Infect Dis. 1998; 178: 1327-1333
- Shapiro RL, et al.:Antiviral Therapy. 2013; 18: 585-590
- 矢野 邦夫ほか:化学療法の領域. 2008; 24: 87-98
- van Leeuwen R, et al.:J Infect Dis. 1995; 171: 1166-1171
- Chittick GE, et al.:Pharmacotherapy. 1999; 19: 932-942
- Yuen GJ, et al.:Clin Pharmacokinet. 2008; 47: 351-371
- McDowell JA, et al.:Antimicrob Agents Chemother. 1999; 43: 2855-2861
- Johnson MA, et al.:Clin Pharmacokinet. 1999; 36: 41-66
- Heald AE, et al.:Antimicrob Agents Chemother. 1996; 40: 1514-1519
- Thompson M, et al.:Abstracts of the 12th World AIDS Conference. 1998; Abstract 42278
- Johnson MA, et al.:Eur J Clin Pharmacol. 1998; 54: 363-366
- Raffi F, et al.:Abstracts of the 40th Interscience Conference on Antimicrobial Agents and Chemotherapy. 2000; Abstract 1630
- McDowell JA, et al.:Antimicrob Agents Chemother. 2000; 44: 1686-1690
- Wang LH, et al.:Antimicrob Agents Chemother. 1999; 43: 1708-1715
- Cammack N, et al.:Biochem Pharmacol. 1992; 43: 2059-2064
- Hart GJ, et al.:Antimicrob Agents Chemother. 1992; 36: 1688-1694
- Coates JAV, et al.:Antimicrob Agents Chemother. 1992; 36: 733-739
- Tisdale M, et al.:Antimicrob Agents Chemother. 1997; 41: 1094-1098
- Faletto MB, et al.:Antimicrob Agents Chemother. 1997; 41: 1099-1107
- Daluge SM, et al.:Antimicrob Agents Chemother. 1997; 41: 1082-1093
- Merrill DP, et al.:J Infect Dis. 1996; 173: 355-364
- Saavedra J, et al.:Abstracts of the 37th Interscience Conference on Antimicrobial Agents and Chemotherapy. 1997; 253
- Schuurman R, et al.:J Infect Dis. 1995; 171: 1411-1419
- Tisdale M, et al.:Proc Natl Acad Sci USA. 1993; 90: 5653-5656
- Back NKT, et al.:EMBO J. 1996; 15: 4040-4049
- Larder BA, et al.:Science. 1995; 269: 696-699
- Maguire M, et al.:AIDS. 2000; 14: 1195-1201
- Kuritzkes DR, et al.:AIDS. 1996; 10: 975-981
- Schinazi RF, et al.:Int Antiviral News. 2000; 8: 65-91
- Miller V, et al.:AIDS. 1998; 12: 705-712
- Johnson MA, et al.:Br J Clin Pharmacol. 1998; 46: 21-27
- Jungmann NA, et al.:Expert Opin Drug Metab Toxicol. 2019; 15: 975-984
- McDowell JA, et al.:Antimicrob Agents Chemother. 2000; 44(8): 2061-2067
- 社内資料:海外臨床試験(204994)
- DeJesus E, et al.:Pulm Circ. 2019; 9(2): 1-10
**24. 文献請求先及び問い合わせ先
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1
ヴィーブヘルスケア・カスタマー・サービス
TEL:0120-066-525(9:00~17:45/土日祝日及び当社休業日を除く)
https://viivhealthcare.com/ja-jp/
26. 製造販売業者等
**26.1 製造販売元
ヴィーブヘルスケア株式会社
東京都港区赤坂1-8-1
**26.2 販売元
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1
■過敏症を注意するカード


