ボカブリア錠30mgの添付文書
- 商品名:
- ボカブリア錠30mg
- 一般名:
- カボテグラビルナトリウム
- 略称 :
- CAB

添付文書の読み方
ここで提供している添付文書情報は、2025年1月現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
HIVインテグラーゼ阻害剤
カボテグラビルナトリウム

- **2024年1月改訂(第4版)
- *2023年8月改訂(第3版)
規制区分:処方箋医薬品注)
注)注意-医師等の処方箋により使用すること
| 日本標準商品分類番号 | 87625 |
|---|
| 貯法 | 室温保存 |
|---|---|
| 有効期間 | 3年 |
| 承認番号 | 30400AMX00201000 |
|---|---|
| 販売開始 | 2022年6月 |
2. 禁忌(次の患者には投与しないこと)
2.1
本剤の成分に対し過敏症の既往歴のある患者
2.2
リファンピシン、フェニトイン、ホスフェニトイン、フェノバルビタール、カルバマゼピンを投与中の患者[10.1参照]
3. 組成・性状
3.1 組成
| 販売名 | ボカブリア錠30mg |
|---|---|
| 有効成分 | 1錠中 カボテグラビルナトリウム31.62mg (カボテグラビルとして30mg) |
| 添加剤 | 乳糖水和物、結晶セルロース、ヒプロメロース、デンプングリコール酸ナトリウム、ステアリン酸マグネシウム、酸化チタン、マクロゴール400 |
3.2 製剤の性状
| 販売名 | ボカブリア錠30mg |
|---|---|
| 剤形・性状 | 白色のフィルムコーティング錠 |
| 識別コード | SV CTV |
| 表 (長径×短径) |
 約14.5mm×約8.1mm |
| 裏 |  |
| 側面 (厚さ) |
 約5.2mm |
| 質量 | 515mg |
4. 効能又は効果
HIV-1感染症
5. 効能又は効果に関連する注意
5.1
本剤は、ウイルス学的失敗の経験がなく、切り替え前6ヵ月間以上においてウイルス学的抑制(ヒト免疫不全ウイルス[HIV]-1 RNA量が50copies/mL未満)が得られており、カボテグラビル及びリルピビリンに対する耐性関連変異を持たず、本剤への切り替えが適切であると判断される抗HIV薬既治療患者に使用すること。[17.1.1-17.1.3参照]
5.2
本剤による治療にあたっては、患者の治療歴及び可能な場合には薬剤耐性検査(遺伝子型解析あるいは表現型解析)を参考にすること。
5.3
本剤は以下の場合に限り使用すること。
- 長時間作用型の薬剤であるカボテグラビル注射剤の投与に先立って、経口導入としてカボテグラビルへの忍容性を確認する。
- カボテグラビル注射剤を予定するスケジュール通りに投与できない場合の代替薬として使用する。
6. 用法及び用量
リルピビリン塩酸塩との併用において、通常、成人には1回1錠(カボテグラビルとして30mg)を1日1回経口投与する。
7. 用法及び用量に関連する注意
7.1
本剤は食事の有無に関わらず投与できるが、リルピビリン経口剤と併用する場合は、食事中又は食直後に経口投与すること。
7.2
カボテグラビル注射剤及びリルピビリン注射剤の併用療法の経口導入として用いる場合には、本剤をリルピビリン経口剤との併用により1ヵ月間(少なくとも28日間)を目安に経口投与し、カボテグラビル及びリルピビリンに対する忍容性を確認すること。
7.3
カボテグラビル注射剤を投与予定日の7日後までに投与できない場合は、本剤による代替投与が可能であるが、以下の点に留意すること。
- 代替投与可能な期間は2ヵ月間までであること。本剤による代替期間が2ヵ月間を超える場合は、他の抗HIV薬へ切り替えることを考慮すること。
- カボテグラビル注射剤を再開する際にはカボテグラビル注射剤の電子添文を参照すること。
8. 重要な基本的注意
8.1
本剤による治療は、抗HIV療法に十分な経験を持つ医師のもとで開始すること。
*8.2
本剤の使用に際しては、国内外のガイドライン等の最新の情報を参考に、患者又は患者に代わる適切な者に、次の事項についてよく説明し同意を得た後、使用すること。
- 本剤はHIV感染症の根治療法薬ではないことから、日和見感染を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので、本剤投与開始後の身体状況の変化については、すべて担当医に報告すること。
- 本剤の長期投与による影響については、現在のところ不明であること。
- 担当医の指示なしに用量を変更したり、服用を中止したりしないこと。
- 本剤は併用薬剤と相互作用を起こすことがあるため、服用中のすべての薬剤を担当医に報告すること。また、本剤で治療中に新たに他の薬剤を服用する場合には、事前に担当医に報告すること。
8.3
肝機能障害があらわれることがあるので、定期的に肝機能検査を行う等、観察を十分に行うこと。[11.1.1参照]
9. 特定の背景を有する患者に関する注意
9.3 肝機能障害患者
9.3.1 重度の肝機能障害(Child-Pugh分類:C)患者
重度(Child-Pugh分類:C)の肝機能障害患者を対象とした臨床試験は実施していない。[11.1.1参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
動物実験(ラット)において、1000mg/kg/日(最大臨床用量におけるヒト曝露量の26倍)の経口投与時に、胎児体重の低値、分娩遅延、死産数の増加及び出生児の生存率低下が報告されている。また、動物実験(ラット)で胎盤通過性が認められている。
9.6 授乳婦
授乳を避けさせること。一般に、乳児へのHIV感染を防ぐため、あらゆる状況下においてHIVに感染した女性は授乳をすべきでない。
動物実験(ラット)において、妊娠6日から分娩20日にカボテグラビルを経口投与したとき、生後10日の出生児血漿中に薬物が認められたことから、ヒトにおいても乳汁に移行する可能性がある。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
10. 相互作用
カボテグラビルは主にUGT1A1で代謝される。また、カボテグラビルはOAT1及びOAT3を阻害する。[16.4.1、16.7.1参照]
10.1 併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| リファンピシン リファジン [2.2、16.7.3参照] |
本剤の血漿中濃度が低下し、本剤の効果が減弱するおそれがある。 | これらの薬剤がUGT1A1を誘導することにより、本剤の代謝が促進される。 |
| カルバマゼピン テグレトール [2.2参照] |
||
| フェニトイン アレビアチン [2.2参照] |
||
| ホスフェニトイン ホストイン [2.2参照] |
||
| フェノバルビタール フェノバール [2.2参照] |
10.2 併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| 制酸剤(Mg、Ca、Al等) 乾燥水酸化アルミニウムゲル 沈降炭酸カルシウム等 |
本剤の血漿中濃度が低下し、本剤の効果が減弱するおそれがある。多価カチオン含有制酸剤は、本剤の投与2時間以上前又は4時間以上後の経口投与が推奨される。 | これらの多価カチオンと錯体を形成することにより、本剤の吸収が阻害される。 |
| メトトレキサート [16.7.1参照] |
メトトレキサートの作用が増強するおそれがあるため、患者の状態を慎重に観察すること。 | 本剤のOAT1/OAT3の阻害作用により、メトトレキサートの血漿中濃度が上昇する可能性がある。 |
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 肝機能障害(頻度不明)
AST、ALTの上昇等を伴う肝機能障害があらわれることがある。[8.3、9.3.1参照]
11.1.2 薬剤性過敏症症候群(頻度不明)
重度又は発熱を伴う発疹、全身倦怠感、疲労、筋肉痛又は関節痛、水疱、口腔病変、結膜炎、顔面浮腫、肝炎、好酸球増加症又は血管性浮腫等があらわれた場合には投与を中止し、肝機能検査を行う等、患者の状態を十分に観察すること。
11.2 その他の副作用
| 1~10%未満 | 1%未満 | 頻度不明 | |
|---|---|---|---|
| 精神・神経系 | 頭痛、不安、異常な夢、不眠症、浮動性めまい | うつ病、傾眠 | 自殺念慮、自殺企図 |
| 消化器 | 悪心、下痢 | 嘔吐、腹痛、鼓腸 | |
| 皮膚 | 発疹 | 血管性浮腫、蕁麻疹 | |
| 筋骨格 | 筋肉痛 | ||
| 全身症状 | 発熱、疲労、無力症、倦怠感 | ||
| 臨床検査 | 体重増加、トランスアミナーゼ上昇、リパーゼ増加 | 総ビリルビン上昇 |
リルピビリン製剤併用時の経口剤及び注射剤における発現頻度
16. 薬物動態
16.1 血中濃度
16.1.1 経口投与(投与1日目)
HIV感染症患者8例にカボテグラビル30mgを1日1回反復経口投与した時の投与初日の薬物動態パラメータ及び血漿中濃度推移をそれぞれ表-1及び図-1に示す1)。
| AUC(0-t) (μg・h/mL) |
Cmax (μg/mL) |
C24 (μg/mL) |
tmax (h)注1) |
|---|---|---|---|
| 70.1038 (10.68865) |
4.6963 (0.82365) |
2.2475 (0.33835) |
2.9333 (0.983 - 4.000) |
平均値(標準偏差)、8例
注1)中央値(範囲)
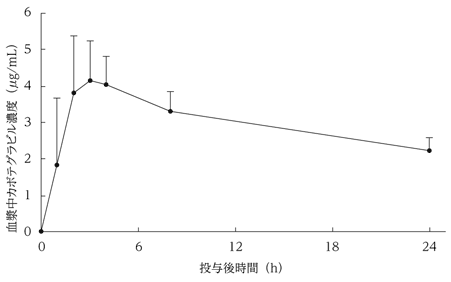
(平均値+標準偏差、8例)
16.1.2 反復経口投与
(1)
母集団薬物動態モデルを用いた、HIV感染症患者を対象とした国際共同第III相試験(201584試験及び201585試験)におけるカボテグラビルとリルピビリン併用投与時のカボテグラビルの薬物動態パラメータ(推定値)を日本人及び外国人集団別に表-2に示す。[17.1.1、17.1.2参照]
薬物動態パラメータについては、カボテグラビル30mgを1日1回反復経口投与した時の実測値に基づく各被験者の事後推定値を踏まえて予測した結果である。
| 患者 | 例数 | AUC(0-τ) (µg・h/mL) |
Cmax (µg/mL) |
Cτ (µg/mL) |
tmax注1) (h) |
|---|---|---|---|---|---|
| 日本人 | 8 | 185.7 (165, 209) |
9.6 (8.6, 10.7) |
6.1 (5.4, 7) |
2.8 (1.2 - 4.7) |
| 外国人 | 732 | 146.7 (143.7, 149.7) |
8.0 (7.9, 8.2) |
4.7 (4.6, 4.8) |
1.9 (1.5 - 4.9) |
幾何平均値(95%信頼区間)
注1)中央値(範囲)
(2)
HIV感染症患者8例にカボテグラビル30mgを1日1回反復経口投与した時、血漿中カボテグラビル濃度は投与7日後までに定常状態に達した2)(外国人データ)。
16.2 吸収
16.2.1 食事の影響
健康成人21例に食後(高脂肪食:53%脂肪/870kcal)に本剤30mgを単回経口投与注)した時、空腹時と比べて、血漿中カボテグラビルのAUC(0-t)及びCmaxはいずれも14%増加した3)(外国人データ)。
16.2.2 バイオアベイラビリティ
カボテグラビルの経口剤と注射剤(筋肉内投与)を比較した時の経口剤の相対バイオアベイラビリティは75.6%であった(母集団薬物動態解析による推定値)。
16.3 分布
16.3.1 血漿蛋白結合率
In vitroでのカボテグラビルのヒト血漿蛋白結合率は99%超であった4)。
16.3.2 分布容積
カボテグラビルの見かけの分布容積(幾何平均値)は12.3Lであった3)。
16.3.3 血球移行性
ヒトでの血液:血漿の比(平均値)は0.437~0.571であった5)。
16.3.4 脳脊髄液への移行
カボテグラビルは脳脊髄液中に分布する。HIV感染症患者にカボテグラビル400mgを4週間隔で、カボテグラビル600mgを8週間隔で筋肉内投与注)した時、定常状態における投与1週間後のカボテグラビルの脳脊髄液中濃度と血漿中濃度との比(中央値)はいずれも0.003であった6)(外国人データ)。
16.3.5 組織内分布
カボテグラビルは男性及び女性の生殖器に分布する。健康成人にカボテグラビル400mgを単回筋肉内投与注)した時、子宮頸部及び膣組織:血漿比の中央値は0.16~0.28、直腸組織:血漿比の中央値は0.08以下であった7)(外国人データ)。
16.4 代謝
16.4.1 主な代謝酵素
In vitroにおいてカボテグラビルは主にUGT1A1で、一部UGT1A9でグルクロン酸抱合された8)。[10.参照]
16.5 排泄
健康成人に14C-カボテグラビル30mg(水溶液)注)を単回経口投与した時の総投与量の約59%が糞中に、約27%が尿中に回収された。糞中排泄物の大部分(総投与量の約47%)は未変化体であり、尿中には代謝物のみ検出された5)(外国人データ)。
16.6 特定の背景を有する患者
16.6.1 腎機能障害患者
重度の腎機能低下者(8例、クレアチニンクリアランス(Ccr):30mL/min未満)及び健康成人8例にカボテグラビル30mgを単回経口投与した時の血漿中カボテグラビルの薬物動態パラメータを表-3に示す9)(外国人データ)。なお、透析患者でのカボテグラビルの薬物動態に及ぼす影響については検討していない。
| 被験者 | 例数 | Cmax (µg/mL) |
AUC(0-inf) (µg·h/mL) |
t1/2 (h) |
|---|---|---|---|---|
| 重度の腎機能低下者 | 8 | 3.34 (2.67, 4.17) |
142.72注1) (115.40, 176.51) |
39.24注1) (33.93, 45.39) |
| 健康成人 | 8 | 3.37 (2.96, 3.83) |
140.48 (115.84, 170.37) |
40.54 (36.92, 44.52) |
幾何平均値(95%信頼区間)
注1)7例
16.6.2 肝機能障害患者
中等度の肝機能低下者(8例、Child-Pugh分類:B)及び健康成人8例にカボテグラビル30mgを単回経口投与した時の血漿中カボテグラビルの薬物動態パラメータを表-4に示す10)(外国人データ)。なお、重度の肝機能低下者でのカボテグラビルの薬物動態に及ぼす影響については検討していない。
| 被験者 | 例数 | Cmax (µg/mL) |
AUC(0-inf) (µg·h/mL) |
t1/2 (h) |
|---|---|---|---|---|
| 中等度の肝機能低下者 | 8 | 2.70 (1.94,3.76) |
101.73 (75.22, 137.58) |
30.85 (23.72, 40.13) |
| 健康成人 | 8 | 3.55 (2.90, 4.33) |
127.08 (94.74, 170.47) |
37.25 (33.41, 41.53) |
幾何平均値(95%信頼区間)
16.7 薬物相互作用
16.7.1 In vitro試験
In vitroにおいてカボテグラビルはP-gp及びBCRPの基質であった11),12)。また、in vitroにおいてカボテグラビルはOAT1及びOAT3を阻害し、IC50はそれぞれ0.81及び0.41µMであった13)。[10.、10.2参照]
16.7.2 カボテグラビルが併用薬の薬物動態に及ぼす影響
カボテグラビルが併用薬の薬物動態に及ぼす影響を表-5に示す(外国人データ)。
| 併用薬及び用量 | カボテグラビルの用量 | 例数 | カボテグラビル併用時/非併用時の併用薬の 薬物動態パラメータの幾何平均の比 (90%信頼区間) |
||
|---|---|---|---|---|---|
| Cmax | AUC | Cτ又はC24 | |||
| エチニルエストラジオール 0.03mg 1日1回14) |
30mg注1) | 19 | 0.92 (0.83, 1.03) |
1.02 (0.97, 1.08) |
1.00 (0.92, 1.10) |
| レボノルゲストレル 0.15mg 1日1回14) |
30mg注1) | 19 | 1.05 (0.96, 1.15) |
1.12 (1.07, 1.18) |
1.07 (1.01, 1.15) |
| ミダゾラム 3mg単回15) |
30mg注1) | 12 | 1.09 (0.94, 1.26) |
1.08 (0.96, 1.22) |
- |
| リルピビリン 25mg 1日1回16) |
30mg注1) | 11 | 0.96 (0.85, 1.09) |
0.99 (0.89, 1.09) |
0.92 (0.79, 1.07) |
算出不能:-
注1)カボテグラビル経口剤1日1回投与時
16.7.3 併用薬がカボテグラビルの薬物動態に及ぼす影響
併用薬がカボテグラビルの薬物動態に及ぼす影響を表-6に示す(外国人データ)。[10.1参照]
| 併用薬及び用量 | カボテグラビルの用量 | 例数 | 他剤併用時/非併用時のカボテグラビルの 薬物動態パラメータの幾何平均の比 (90%信頼区間) |
||
|---|---|---|---|---|---|
| Cmax | AUC | Cτ又はC24 | |||
| エトラビリン 200mg 1日2回17) |
30mg注1) | 12 | 1.04 (0.99, 1.09) |
1.01 (0.96, 1.06) |
1.00 (0.94, 1.06) |
| リファブチン 300mg 1日1回18) |
30mg注1) | 12 | 0.83 (0.76, 0.90) |
0.79 (0.74, 0.83) |
0.74 (0.70, 0.78) |
| リファンピシン 600mg 1日1回19) |
30mg注2) | 15 | 0.94 (0.87, 1.02) |
0.41 (0.36, 0.46) |
0.50 (0.44, 0.57) |
| リルピビリン 25mg 1日1回16) |
30mg注1) | 11 | 1.05 (0.96, 1.15) |
1.12 (1.05, 1.19) |
1.14 (1.04, 1.24) |
- 注1)カボテグラビル経口剤1日1回投与時
- 注2)カボテグラビル経口剤単回投与時
注)本剤の承認された用法及び用量は、「リルピビリン塩酸塩との併用において、通常、成人には1回1錠(カボテグラビルとして30mg)を1日1回経口投与する。」である。
17. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第III相試験(FLAIR:201584試験)
抗レトロウイルス療法による治療経験のない成人HIV-1感染症患者を対象にインテグラーゼ阻害剤(INSTI)を含む1日1回1錠のレジメンからカボテグラビルとリルピビリンの併用療法に切り替えた後のウイルス学的抑制の維持の評価を目的としたランダム化非盲検比較試験に629例が組み入れられた。組み入れられた被験者にドルテグラビル・アバカビル・ラミブジン配合錠[HLA-B*5701陽性被験者では、ドルテグラビルと核酸系逆転写酵素阻害剤(NRTI)2剤]を1日1回、20週間経口投与した。HIV-1 RNA量が50copies/mL未満であった被験者566例(日本人患者20例を含む)のうち、カボテグラビルとリルピビリンの併用投与群(CAB+RPV群)に283例、ドルテグラビル・アバカビル・ラミブジン配合錠[HLA-B*5701陽性被験者では、ドルテグラビルと核酸系逆転写酵素阻害剤(NRTI)2剤]を継続する群(継続投与群)に283例が割り付けられた。CAB+RPV群に割り付けられた被験者には、カボテグラビル経口剤30mgとリルピビリン経口剤25mgを1日1回、少なくとも4週間併用経口投与した後、カボテグラビル注射剤(1ヵ月目600mg、2ヵ月目以降400mg)とリルピビリン注射剤(1ヵ月目900mg、2ヵ月目以降600mg)を1ヵ月間隔で44週間臀部筋肉内に併用投与した20)。両群の患者背景及び疾患特性に偏りはみられずCAB+RPV群の年齢中央値は34歳(範囲19-68歳)、女性22%、人種は白人76%、黒人又はアフリカ系アメリカ人17%、アジア人4%、その他が3%であった。ベースラインのCD4陽性リンパ球数350cells/mm3未満は7%であった。
主要評価項目である投与48週時のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、継続投与群の2.5%に対して、CAB+RPV群で2.1%であり、調整した群間差の95%信頼区間の上限値(2.1%)は、非劣性マージン(6%)より小さく、継続投与群に対するCAB+RPV群の非劣性が示された。48週時までにウイルス学的失敗の基準(HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上)を満たした被験者はCAB+RPV群で1.4%(4/283例)、継続投与群で1.1%(3/283例)であった。48週時のベースライン特性別のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、CAB+RPV群及び継続投与群で同程度であった。日本人集団における主要評価項目である投与48週時のHIV-1 RNA量が50copies/mL以上であった被験者は、CAB+RPV群(8例)及び継続投与群(12例)両群ともに0例であった。[5.1、16.1.2参照]
副作用発現頻度は、CAB+RPV群で83%(236/283例)であった。主な副作用は、注射部位疼痛78%(221/283例)、注射部位結節15%(43/283例)、注射部位硬結13%(37/283例)、注射部位腫脹8%(22/283例)、注射部位そう痒感6%(16/283例)、頭痛5%(14/283例)、発熱5%(13/283例)、注射部位紅斑4%(12/283例)、注射部位熱感3%(8/283例)及び体温上昇3%(8/283例)であった。日本人集団において2例以上にみられた副作用は、注射部位疼痛88%(7/8例)、倦怠感38%(3/8例)であった。
なお、本試験における試験成績の要約を表-1に、ベースラインの特性別の48週時のHIV-1 RNA量が50copies/mL以上の被験者の割合を表-2に示した。
| CAB+RPV群 283例 |
継続投与群 283例 |
|
|---|---|---|
| HIV-1 RNA量が50copies/mL以上注1) | 6例(2.1%) | 7例(2.5%) |
| 両群間の差(95%信頼区間)注2) | -0.4%(-2.8%, 2.1%) | |
| ウイルス学的失敗注3) | 4例(1.4%)注4) | 3例(1.1%) |
- 注1)有効性の欠如による中止及びウイルス学的抑制が得られていない期間中に中止した症例を含む
- 注2)ベースラインの層別因子により調整
- 注3)HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上
- 注4)CAB+RPV群の4例のうち3例は、サブタイプA1であり、残りの1例はCAB+RPVの併用投与を受けていなかった
| CAB+RPV群 283例 |
継続投与群 283例 |
|
|---|---|---|
| ベースラインCD4陽性リンパ球数(cells/mm3) | ||
| <350 | 0/19 | 1/27(3.7%) |
| 350-<500 | 3/64(4.7%) | 0/60 |
| ≥500 | 3/200(1.5%) | 6/196(3.1%) |
| 性別 | ||
| 男性 | 3/220(1.4%) | 6/219(2.7%) |
| 女性 | 3/63(4.8%) | 1/64(1.6%) |
| 人種 | ||
| 白人 | 6/216(2.8%) | 5/201(2.5%) |
| 黒人/アフリカ系アメリカ人 | 0/47 | 2/56(3.6%) |
| アジア人 | 0/12 | 0/15 |
| その他 | 0/8 | 0/9 |
| BMI(kg/m2) | ||
| <30 | 3/243(1.2%) | 7/246(2.8%) |
| ≥30 | 3/40(7.5%) | 0/37 |
| 年齢(歳) | ||
| <50 | 5/250(2.0%) | 6/254(2.4%) |
| ≥50 | 1/33(3.0%) | 1/29(3.4%) |
17.1.2 海外第III相試験(ATLAS:201585試験)
抗レトロウイルス療法により、少なくとも6ヵ月間ウイルス学的に抑制されている成人HIV-1感染症患者616例を対象としたランダム化非盲検試験において、カボテグラビルとリルピビリンの併用投与群(CAB+RPV群)に308例、現行のレジメンを継続する群(継続投与群)に308例が割り付けられた。CAB+RPV群に割り付けられた被験者には、カボテグラビル経口剤30mgとリルピビリン経口剤25mgを1日1回、少なくとも4週間併用経口投与した後、カボテグラビル注射剤(1ヵ月目600mg、2ヵ月目以降400mg)とリルピビリン注射剤(1ヵ月目900mg、2ヵ月目以降600mg)を1ヵ月間隔で44週間臀部筋肉内に併用投与した21)。両群の患者背景及び疾患特性に偏りはみられずCAB+RPV群の年齢中央値は40歳(範囲21-74歳)、女性32%、人種は白人69%、黒人又はアフリカ系アメリカ人20%、アジア人7%、その他が3%であった。ベースラインのCD4陽性リンパ球数350cells/mm3未満は7%であった。
主要評価項目である投与48週時のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、継続投与群の1.0%に対して、CAB+RPV群で1.6%であり、調整した群間差の95%信頼区間の上限値(2.5%)は、非劣性マージン(6%)より小さく、継続投与群に対するCAB+RPV群の非劣性が示された。48週時までにウイルス学的失敗の基準(HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上)を満たした被験者はCAB+RPV群で1.0%(3/308例)、継続投与群で1.3%(4/308例)であった。48週時のベースライン特性別のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、CAB+RPV群及び継続投与群で同程度であった。[5.1、16.1.2参照]
副作用発現頻度は、CAB+RPV群で83%(255/308例)であった。主な副作用は、注射部位疼痛74%(227/308例)、注射部位結節12%(36/308例)、注射部位硬結9%(29/308例)、注射部位腫脹7%(22/308例)、注射部位紅斑4%(12/308例)、疲労4%(11/308例)、発熱4%(11/308例)、注射部位内出血3%(10/308例)、悪心4%(11/308例)、頭痛4%(11/308例)及び不眠症3%(8/308例)であった。
なお、本試験における試験成績の要約を表-3に、ベースラインの特性別の48週時のHIV-1 RNA量が50copies/mL以上の被験者の割合を表-4に示した。
| CAB+RPV群 308例 |
継続投与群 308例 |
|
|---|---|---|
| HIV-1 RNA量が50copies/mL以上注1) | 5例(1.6%) | 3例(1.0%) |
| 両群間の差(95%信頼区間)注2) | 0.6%(-1.2%, 2.5%) | |
| ウイルス学的失敗注3) | 3例(1.0%)注4) | 4例(1.3%) |
- 注1)有効性の欠如による中止及びウイルス学的抑制が得られていない期間中に中止した症例を含む
- 注2)ベースラインの層別因子により調整
- 注3)HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上
- 注4)CAB+RPV群の3例は、サブタイプA、A1及びAGであった
| CAB+RPV群 308例 |
継続投与群 308例 |
|
|---|---|---|
| ベースラインCD4陽性リンパ球数(cells/mm3) | ||
| <350 | 0/23 | 1/27(3.7%) |
| 350-<500 | 2/56(3.6%) | 0/57 |
| ≥500 | 3/229(1.3%) | 2/224(0.9%) |
| 性別 | ||
| 男性 | 3/209(1.4%) | 3/204(1.5%) |
| 女性 | 2/99(2.0%) | 0/104 |
| 人種 | ||
| 白人 | 3/214(1.4%) | 2/207(1.0%) |
| 黒人/アフリカ系アメリカ人 | 2/62(3.2%) | 1/77(1.3%) |
| アジア人 | 0/22 | 0/13 |
| その他 | 0/10 | 0/11 |
| BMI(kg/m2) | ||
| <30 | 3/248(1.2%) | 1/242(0.4%) |
| ≥30 | 2/60(3.3%) | 2/66(3.0%) |
| 年齢(歳) | ||
| <50 | 4/242(1.7%) | 2/212(0.9%) |
| ≥50 | 1/66(1.5%) | 1/96(1.0%) |
| ランダム化時の継続投与 | ||
| PI | 1/51(2.0%) | 0/54 |
| INSTI | 0/102 | 2/99(2.0%) |
| NNRTI | 4/155(2.6%) | 1/155(0.6%) |
PI=プロテアーゼ阻害剤、INSTI=インテグラーゼ阻害剤、NNRTI=非核酸系逆転写酵素阻害剤
17.1.3 海外第III相試験(ATLAS-2M:207966試験)
抗レトロウイルス療法により、ウイルス学的に抑制されている成人HIV-1感染症患者1045例を対象としたランダム化非盲検試験において、カボテグラビルとリルピビリンを1ヵ月間隔で併用投与する群(1ヵ月間隔投与群)に523例、2ヵ月間隔で併用投与する群(2ヵ月間隔投与群)に522例が割り付けられた。
割付け前にカボテグラビルとリルピビリンの併用療法以外の治療を受けていた被験者には、カボテグラビル経口剤30mgとリルピビリン経口剤25mgを1日1回、少なくとも4週間併用経口投与した。1ヵ月間隔投与群では、カボテグラビル注射剤(1ヵ月目600mg、2ヵ月目以降1ヵ月間隔で400mg)とリルピビリン注射剤(1ヵ月目900mg、2ヵ月目以降1ヵ月間隔で600mg)を44週間臀部筋肉内に併用投与した。2ヵ月間隔投与群では、カボテグラビル注射剤(1、2ヵ月目及び以降2ヵ月間隔で600mg)とリルピビリン注射剤(1、2ヵ月目及び以降2ヵ月間隔で900mg)を44週間臀部筋肉内に併用投与した22)。1ヵ月間隔投与群及び2ヵ月間隔投与群の患者背景及び疾患特性に偏りはみられず、年齢の中央値はいずれも42.0歳、性別は両群ともに男性が70%以上で、人種も70%以上が白人であり、CD4陽性リンパ球数350cells/mm3未満は、それぞれ5%及び7%であった。
主要評価項目である投与48週時のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、1ヵ月間隔投与群の1.0%に対して、2ヵ月間隔投与群で1.7%であり、調整した群間差の95%信頼区間の上限値(2.2%)は、非劣性マージン(4%)より小さく、1ヵ月間隔投与群に対する2ヵ月間隔投与群の非劣性が示された。48週時までにウイルス学的失敗の基準(HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上)を満たした被験者は1ヵ月間隔投与群で0.4%(2/523例)、2ヵ月間隔投与群で1.5%(8/522例)であった。48週時のベースライン特性別のHIV-1 RNA量が50copies/mL以上であった被験者の割合は、両群で同程度であった。[5.1参照]
副作用発現頻度は、1ヵ月間隔投与群で76%(399/523例)、2ヵ月間隔投与群で77%(400/522例)であった。1ヵ月間隔投与群の主な副作用は、注射部位疼痛68%(358/523例)、注射部位結節17%(87/523例)、注射部位硬結7%(37/523例)、注射部位不快感8%(40/523例)、注射部位腫脹5%(26/523例)、発熱5%(25/523例)、注射部位そう痒感5%(24/523例)、疲労4%(19/523例)、注射部位紅斑3%(15/523例)及び注射部位血腫3%(14/523例)であり、2ヵ月間隔投与群の主な副作用は、注射部位疼痛70%(364/522例)、注射部位結節10%(54/522例)、注射部位硬結8%(40/522例)、注射部位不快感7%(34/522例)、注射部位腫脹6%(32/522例)、注射部位そう痒感5%(26/522例)及び発熱4%(19/522例)であった。
なお、本試験における試験成績の要約を表-5に、ベースラインの特性別の48週時のHIV-1 RNA量が50copies/mL以上の被験者の割合を表-6に示した。
| 1ヵ月間隔投与群 523例 |
2ヵ月間隔投与群 522例 |
|
|---|---|---|
| HIV-1 RNA量が50copies/mL以上注1) | 5例(1.0%) | 9例(1.7%) |
| 両群間の差(95%信頼区間)注2) | 0.8%(-0.6%, 2.2%) | |
| ウイルス学的失敗注3) | 2例(0.4%)注4) | 8例(1.5%)注4) |
- 注1)有効性の欠如による中止及びウイルス学的抑制が得られていない期間中に中止した症例を含む
- 注2)ベースラインの層別因子により調整
- 注3)HIV-1 RNA量が200copies/mL未満に抑制された後、2回の連続するHIV-1 RNA量の測定結果が200copies/mL以上
- 注4)ウイルス学的失敗の基準を満たした10例のHIV-1サブタイプは、A(2例)、A1(2例)、B(4例)、C(1例)又はComplex(1例)であった
| 1ヵ月間隔投与群 523例 |
2ヵ月間隔投与群 522例 |
|
|---|---|---|
| ベースラインCD4陽性リンパ球数(cells/mm3) | ||
| <350 | 1/27(3.7%) | 1/35(2.9%) |
| 350-<500 | 0/89 | 1/96(1.0%) |
| ≥500 | 4/407(1.0%) | 7/391(1.8%) |
| 性別 | ||
| 男性 | 5/380(1.3%) | 4/385(1.0%) |
| 女性 | 0/143 | 5/137(3.6%) |
| 人種 | ||
| 白人 | 5/393(1.3%) | 5/370(1.4%) |
| 非白人 | 0/130 | 4/152(2.6%) |
| 黒人/アフリカ系アメリカ人 | 0/90 | 4/101(4.0%) |
| 非黒人/アフリカ系アメリカ人 | 5/433(1.2%) | 5/421(1.2%) |
| BMI(kg/m2) | ||
| <30 | 3/425(0.7%) | 3/409(0.7%) |
| ≥30 | 2/98(2.0%) | 6/113(5.3%) |
| 年齢(歳) | ||
| <35 | 1/145(0.7%) | 4/137(2.9%) |
| 35-<50 | 2/239(0.8%) | 3/242(1.2%) |
| ≥50 | 2/139(1.4%) | 2/143(1.4%) |
| CAB+RPV投与歴(週) | ||
| 0 | 5/327(1.5%) | 5/327(1.5%) |
| 1-24 | 0/68 | 3/69(4.3%) |
| >24 | 0/128 | 1/126(0.8%) |
18. 薬効薬理
18.1 作用機序
カボテグラビルはレトロウイルスの複製に必要な酵素であるHIVインテグラーゼの活性部位に結合してその活性を阻害し、ウイルスDNAの宿主DNAへの組込みを抑制する。
18.2 抗ウイルス作用
野生型HIV-1 Ba-L株を感染させた末梢血単核球を用いた時のカボテグラビルのウイルス複製に対する50%阻害濃度(IC50)は0.22nMであった。24種類のHIV-1臨床分離株[グループM(サブタイプA、B、C、D、E、F及びG;それぞれ3種類ずつ)及びグループO;3種類]を感染させた細胞を用いた時のカボテグラビルのIC50は0.02~1.06nMであり、3種類のHIV-2臨床分離株に対するIC50は0.10~0.14nMであった。
HIV-1 IIIB株を感染させたMT-4細胞において、カボテグラビルをリルピビリン、ラミブジン、テノホビル又はエムトリシタビンと併用した時の抗ウイルス活性には、いずれも相加又は相乗効果が認められた。
18.3 薬剤耐性
18.3.1 非臨床試験成績
HIV-1 IIIB株(T124A多型を有する)をカボテグラビル存在下で112日間継代培養した試験で新たに認められたインテグラーゼ領域のアミノ酸変異はQ146L、S153Y及びI162Mであり、感受性変化度[Fold Change(FC):各変異を有する株に対するIC50/野生型HIV-1 NL432株に対するIC50]はそれぞれ1.3~4.6、2.8~8.4及び2.8であった。野生型HIV-1 NL432株をカボテグラビルの存在下で56日間継代培養した試験ではインテグラーゼ領域にアミノ酸変異は認められなかった。
18.3.2 臨床試験成績
201584(FLAIR)試験のCAB+RPV群において、耐性データの得られたウイルス学的失敗例3例中2例では、治療中にINSTI耐性関連Q148R変異を生じており、1例ではカボテグラビルに対する感受性低下を示すG140R変異が生じた。また、3例すべての被験者で1種類のリルピビリン耐性関連変異(K101E、E138E/A/K/T又はE138K)を生じており、3例中2例でリルピビリンに対する感受性の低下を示した。
201585(ATLAS)試験のウイルス学的失敗例3例中1例ではウイルス学的失敗の疑い時にINSTI耐性関連N155H変異が検出された。また、3例すべての被験者で治療中にリルピビリン耐性関連変異(E138A、E138E/K又はE138K)を生じており、リルピビリンに対する感受性の低下を示し、3例中1例はカボテグラビルに対する感受性の低下を示した。
カボテグラビルに対する耐性関連変異は、G140R(1例)、Q148R(2例)及びN155H(1例)であった。
207966(ATLAS-2M)試験において、1ヵ月間隔投与群のウイルス学的失敗例(2例)では、いずれの被験者もベースライン時にリルピビリン又はINSTI耐性関連変異を有していなかった。1例で非核酸系逆転写酵素阻害剤(NNRTI)関連変異(G190Q)とNNRTI多型(V189I)が同時に検出された。ウイルス学的失敗の疑い時に1例で治療中にリルピビリン耐性関連変異(K101E + M230L)が検出され、別の被験者ではNNRTI関連変異(G190Q + V189I)にV179V/Iが追加されていた。いずれの被験者においてもリルピビリンに対する感受性の低下を示した。また、いずれの被験者もウイルス学的失敗の疑い時にINSTI耐性関連変異(Q148R + E138E/K又はN155N/H)を有しており、1例ではカボテグラビルに対する感受性の低下を示した。いずれもINSTI関連変異であるL74Iは有しておらず、これらの被験者におけるカボテグラビルの感受性変化度は1.8~4.6であった。2ヵ月間隔投与群のウイルス学的失敗例(8例)において、ベースライン時に5例がリルピビリン耐性関連変異(Y181Y/C + H221H/Y、Y188Y/F/H/L、Y188L、E138A又はE138E/A)を有し、1例がカボテグラビル耐性関連変異(G140G/R)を有していた(リルピビリン耐性関連変異Y181Y/F/H/Lを有していた症例と同一)。ウイルス学的失敗の疑い時に6例がリルピビリン耐性関連変異を有しており、うち2例でK101E、1例でE138E/Kがベースライン時から追加されていた。リルピビリンの感受性変化度は7例の被験者で生物学的カットオフ値を上回っていた(範囲:2.4~15)。リルピビリン耐性関連変異を有していた6例中5例がINSTI耐性関連変異[N155H(2例)、Q148R(1例)及びQ148Q/R + N155N/H(2例)]を有していた。INSTI耐性関連変異であるL74Iが7例中4例の被験者でみられた。1例の被験者は、インテグラーゼ遺伝子型及び表現型アッセイの結果が得られず、他の1例ではカボテグラビル表現型の結果が得られなかった。これらの被験者におけるカボテグラビルの感受性変化度の範囲は0.6~9.1であった。
18.4 交差耐性
INSTIに対する耐性関連変異(G118R、Q148K、Q148R、T66K/L74M、E92Q/N155H、E138A/Q148R、E138K/Q148K/R、G140C/Q148R、G140S/Q148H/K/R、Y143H/N155H及びQ148R/N155H)を導入したHIV-1 NL432株において、カボテグラビルに対する感受性の低下(野生型NL432株に対するIC50と比較することにより算出した感受性変化度が5以上)が認められた。そのうち、Q148K又はQ148Rを含む複数の変異を導入した場合に顕著な感受性の低下が認められ、N155H/Q148R及びE138K/Q148Kでの感受性変化度はそれぞれ61及び81であった。
カボテグラビルはNNRTI耐性関連変異(K103N及びY188L)及びNRTI耐性関連変異(M184V、D67N/K70R/T215Y及びV75I/F77L/F116Y/Q151M)を有する変異株に対して抗ウイルス活性を示した。
19. 有効成分に関する理化学的知見
| 一般的名称 | カボテグラビルナトリウム(Cabotegravir Sodium) |
|---|---|
| 化学名 | Monosodium(3S,11aR)-8-{[(2,4-difluorophenyl)methyl]carbamoyl}-3-methyl-5,7-dioxo-2,3,5,7,11,11a-hexahydrooxazolo[3,2-a]pyrido[1,2-d]pyrazin-6-olate |
| 分子式 | C19H16F2N3NaO5 |
| 分子量 | 427.33 |
| 化学構造式 | 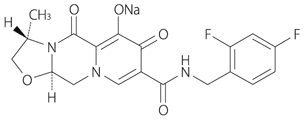 |
| 性状 | 白色の固体 |
| 融点 | 約307℃ |
21. 承認条件
21.1
医薬品リスク管理計画を策定の上、適切に実施すること。
21.2
本剤の使用に当たっては、患者に対して本剤に関して更なる有効性・安全性のデータを引き続き収集中であること等を十分に説明し、インフォームドコンセントを得るよう、医師に要請すること。
21.3
現在実施中又は計画中の臨床試験については、終了後速やかに試験成績及び解析結果を提出すること。
21.4
再審査期間が終了するまでの間、原則として国内の全投与症例を対象とした製造販売後調査を実施し、本剤の使用実態に関する情報(患者背景、有効性・安全性(他剤併用時の有効性・安全性を含む)及び薬物相互作用のデータ等)を収集して定期的に報告するとともに、調査の結果を再審査申請時に提出すること。
22. 包装
30錠[瓶、バラ]
23. 主要文献
- 社内資料:国際共同第III相試験(201584)
- 社内資料:海外臨床試験(ITZ111451、2022年5月31日承認、CTD2.7.2.2.6.3.3)
- 社内資料:海外臨床試験(205696、2022年5月31日承認、CTD2.7.1.2.3.1)
- 社内資料:分布に関する試験(2015N235936、2022年5月31日承認、CTD2.6.4.4.1.1)
- 社内資料:海外臨床試験(LAI117008、2022年5月31日承認、CTD2.7.2.1.2、2.7.2.2.6.1.2)
- 社内資料:海外臨床試験(200056、2022年5月31日承認、CTD2.7.2.2.1.2.5)
- 社内資料:海外臨床試験(LAI114433、2022年5月31日承認、CTD2.7.2.2.3.1.4)
- 社内資料:代謝に関する試験(2012N145430、2022年5月31日承認、CTD2.6.4.5.1.1.5)
- 社内資料:海外臨床試験(201480、2022年5月31日承認、CTD2.7.2.2.6.5.2)
- 社内資料:海外臨床試験(201479、2022年5月31日承認、CTD2.7.2.2.6.5.1)
- 社内資料:分布に関する試験(2012N146040、2022年5月31日承認、CTD2.6.4.4.1.2)
- 社内資料:分布に関する試験(2012N155942、2022年5月31日承認、CTD2.6.4.4.1.4)
- 社内資料:分布に関する試験(2013N174474、2022年5月31日承認、CTD2.6.4.4.1.7)
- 社内資料:海外臨床試験(LAI117011、2022年5月31日承認、CTD2.7.2.2.6.6.4)
- 社内資料:海外臨床試験(LAI116815、2022年5月31日承認、CTD2.7.2.2.6.6.5)
- 社内資料:海外臨床試験(LAI116181、2022年5月31日承認、CTD2.7.2.2.6.6.1)
- 社内資料:海外臨床試験(ITZ111839、2022年5月31日承認、CTD2.7.2.2.6.6.6)
- 社内資料:海外臨床試験(205712、2022年5月31日承認、CTD2.7.2.2.6.6.2)
- 社内資料:海外臨床試験(LAI117010、2022年5月31日承認、CTD2.7.2.2.6.6.3)
- Orkin C,et al.:N Engl J Med.2020;382(12):1124-1135
- Swindells S,et al.:N Engl J Med.2020;382(12):1112-1123
- Overton ET,et al.:Lancet.2020;396:1994-2005
**24. 文献請求先及び問い合わせ先
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1
ヴィーブヘルスケア・カスタマー・サービス
TEL:0120-066-525(9:00~17:45/土日祝日及び当社休業日を除く)
https://viivhealthcare.com/ja-jp/
26. 製造販売業者等
**26.1 製造販売元
ヴィーブヘルスケア株式会社
東京都港区赤坂1-8-1
**26.2 販売元
グラクソ・スミスクライン株式会社
東京都港区赤坂1-8-1