ONCEMRK試験
INDEX
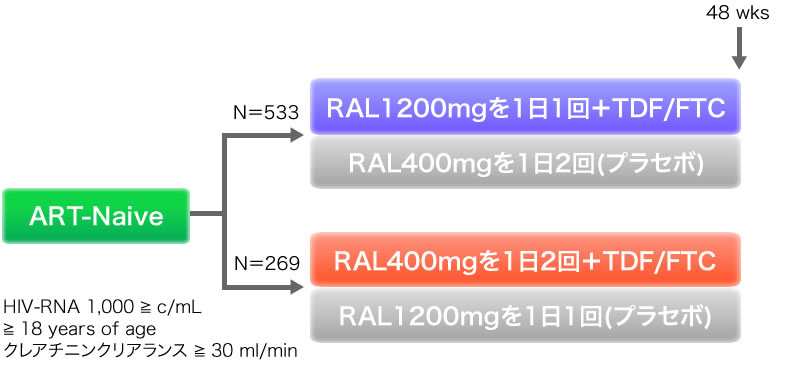
ONCEMRK試験のデザイン(Phase III、無作為化、二重盲検、非劣性試験)
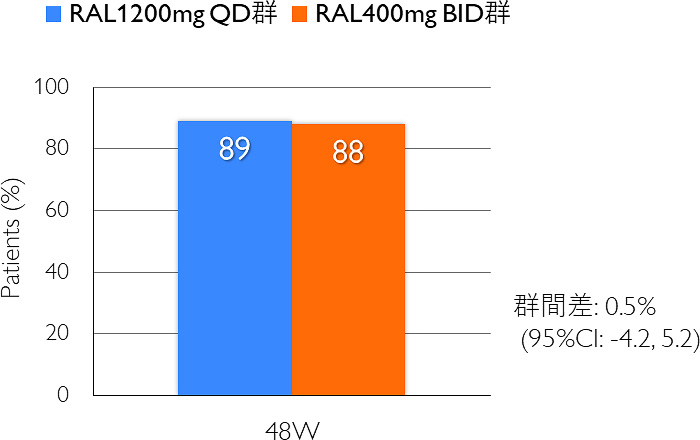
主要評価項目:48週時点でのHIV-RNA量40コピー/mL未満の達成率
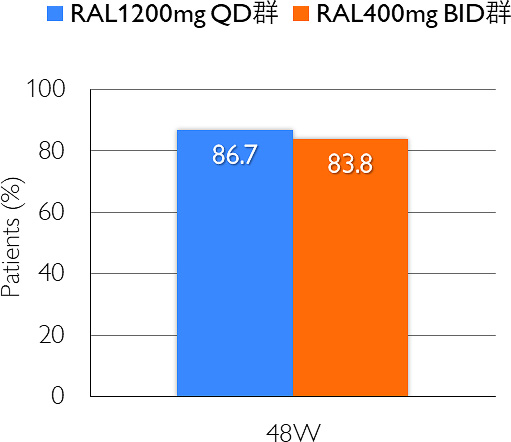
ベースラインのHIV-RNA量が10万コピー以上の患者における40コピー/mL未満の達成率
有害事象
| RAL 1200mg QD群 (n=531) |
RAL 400mg BID群 (n=266) |
||
|---|---|---|---|
| 薬剤関連の有害事象 総数 | 24%(130例) | 26%(68例) | |
| 重篤な有害事象 | <1%(1例) | 1%(2例) | |
| 有害事象による薬剤の中止 | 0 | 1%(2例) | |
| 2%以上の有害事象 | |||
| 消化器症状 | すべて | 14%(76例) | 12%(32例) |
| 腹痛 | 3%(16例) | 1%(2例) | |
| 下痢 | 2%(12例) | 3%(7例) | |
| 悪心 | 7%(39例) | 7%(18例) | |
| 嘔吐 | 2%(13例) | 1%(3例) | |
| 代謝または 栄養上の障害 |
すべて | 3%(14例) | <1%(1例) |
| 食欲減退 | 2%(11例) | 0 | |
| 神経系の障害 | すべて | 7%(38例) | 9%(23例) |
| 非回転性めまい | 2%(12例) | 3%(8例) | |
| 頭痛 | 3%(16例) | 5%(12例) | |
| 精神的な障害 | 4%(20例) | 4%(10例) | |
| 皮膚または皮下組織の障害 | 3%(16例) | 3%(9例) | |
サマリー
未治療の患者に対するRAL1200mgの1日1回投与は、RAL400mgの1日2回投与と比較して、ウイルス抑制効果は48週時点で非劣性であった。
薬剤に関連する有害事象の頻度は両群とも低く、内訳は両群で同様であった。