DRIVE-AHEAD試験
INDEX
DRIVE-AHEAD試験のデザイン(Phase III、無作為化、二重盲検、非劣性試験)
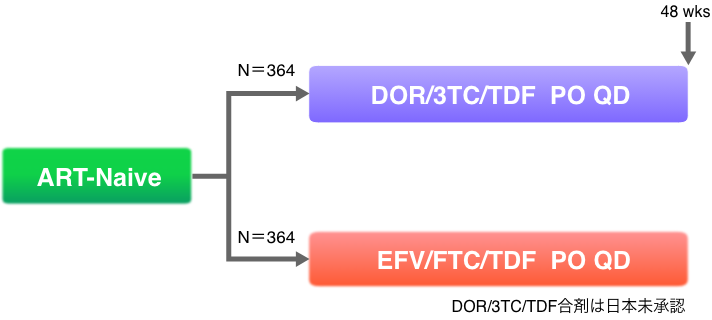
HIV-1 RNA > 1000コピー/mL
本試験のいずれの薬剤にも耐性変異なし
Ccr 50mL/分以上
HIV-1以外のウイルス感染(HBVなど)治療なし
活動性急性肝炎なし.
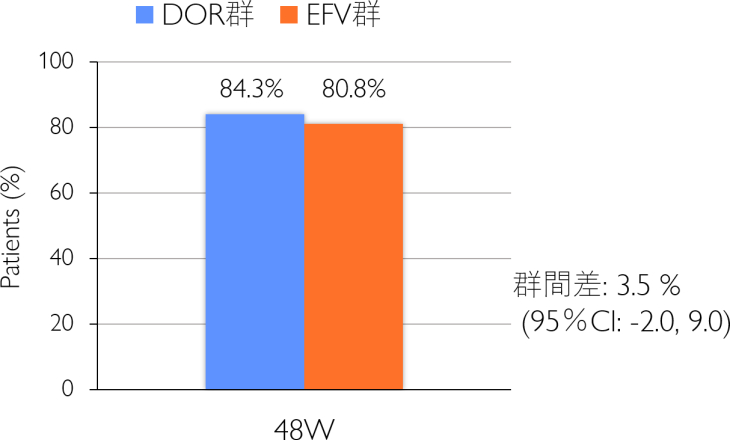
主要評価項目:48週時点でのHIV-RNA量50コピー/mL未満の達成率
有害事象
| DOR群 (n=364) |
EFV群 (n=364) |
||
|---|---|---|---|
| 有害事象 総数(%) | 301例(83%) | 330例(91%) | |
| 5%以上 | 下痢 | 39例(11%) | 49例(13%) |
| 嘔気 | 28例(8%) | 39例(11%) | |
| 嘔吐 | 15例(4%) | 27例(7%) | |
| 疲労 | 21例(6%) | 22例(6%) | |
| 鼻咽頭炎 | 39例(11%) | 31例(9%) | |
| 咽頭炎 | 20例(5%) | 15例(4%) | |
| 上気道感染 | 33例(9%) | 23例(6%) | |
| めまい | 32例(9%) | 135例(37%) | |
| 頭痛 | 47例(13%) | 45例(12%) | |
| 眠気 | 12例(3%) | 27例(7%) | |
| 異夢 | 17例(5%) | 42例(12%) | |
| 不眠 | 19例(5%) | 32例(9%) | |
| 皮疹 | 17例(5%) | 44例(12%) | |
| 薬剤関連の有害事象 | 113例(31%) | 229例(63%) | |
| 重篤な有害事象 | 13例(4%) | 21例(6%) | |
| 薬剤関連 | 1例(<1%) | 4例(1%) | |
| 有害事象による中止 | 11例(3%) | 24例(7%) | |
| 薬剤関連 | 8例(2%) | 21例(6%) | |
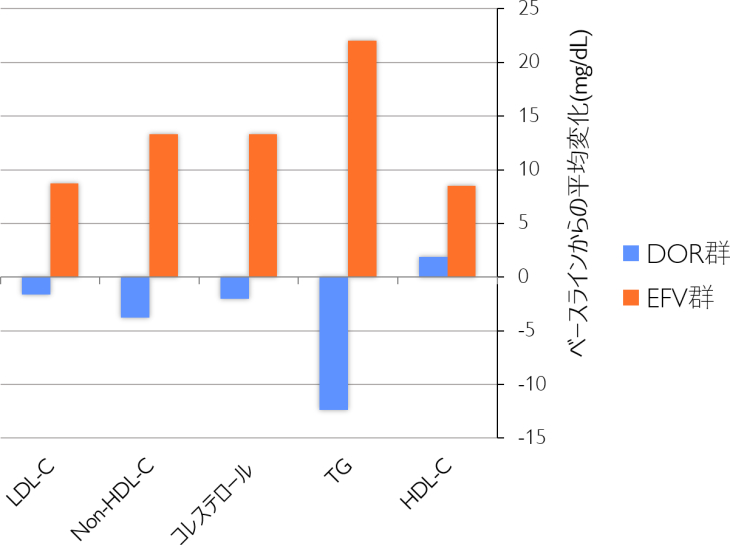
48週後の脂質代謝評価
サマリー
未治療患者を対象とした比較試験において、DOR/3TC/TDF群の48週時点でのウイルス抑制効果は、EFV/FTC/TDF群に対して非劣性であった。CD4数の上昇効果は同様であり、耐性変異の出現率は低かった。
DOR群ではEFV群と比較し神経精神学的有害事象が有意に少なく、脂質に及ぼす影響も少なかった。皮疹の出現率、薬剤関連有害事象、および有害事象による中止も少なかった。
DORの耐性に関する個人的意見
DOR耐性関連変異の出現率はDRIVE-FORWARD試験にて383例中1例(0.3%)DRIVE-AHEAD試験にて363例中7例(1.9%)であり頻度としては低率であった。
しかしながら、高度耐性を含む耐性変異が認められており、アドヒアランス不良な症例への投与は耐性変異獲得の可能性がありうる。